
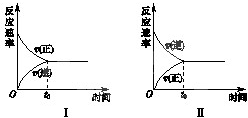
 t��ʱ����������ͬ���ܱո������������ݣ��зֱ����SO2��SO3�ת����ʵ�飬��Ӧ�Ļ�ѧ����ʽΪ2SO2��g��+O2��g��?2SO3��g����ʵ����ʵ��������ֱ���ͼ���ͼ����ʾ��
t��ʱ����������ͬ���ܱո������������ݣ��зֱ����SO2��SO3�ת����ʵ�飬��Ӧ�Ļ�ѧ����ʽΪ2SO2��g��+O2��g��?2SO3��g����ʵ����ʵ��������ֱ���ͼ���ͼ����ʾ��| P |
| 2 |
| P |
| 2 |
| P |
| 2 |
| 1mol/L-a%mol/L |
| 1mol/L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
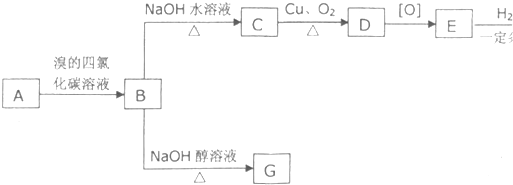
| A������Һ���ɵ����ʵ���Ũ�ȡ��������HCl��Һ��NH3?H2O��Һ��϶��ɸ���Һ |
| B������pH=3��HCl��pH=11��NH3?H2O��Һ�������϶��� |
| C������Һ�����Ӽ����㣺c��Cl-����c��NH4+����c��H+����c��OH-�� ��Һ������һ������NH4Cl |
| D����������NH3?H2O����Һ������Ũ�ȿ���Ϊ��c��NH4+����c��Cl-����c��H+����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
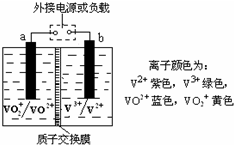 ij���ܵ�ص�ԭ����ͼ��ʾ����Һ��c��H+��=2.0mol?L-1��������ΪSO42-��a��b��Ϊ���Ե缫���������������Һ��ɫ����ɫ��Ϊ��ɫ������������ȷ���ǣ�������
ij���ܵ�ص�ԭ����ͼ��ʾ����Һ��c��H+��=2.0mol?L-1��������ΪSO42-��a��b��Ϊ���Ե缫���������������Һ��ɫ����ɫ��Ϊ��ɫ������������ȷ���ǣ�������| A�����Ҳ���Һ��ɫ����ɫ��Ϊ��ɫʱ�����������ת����ʽΪ��ѧ��ת��Ϊ���� |
| B���������У�a���ķ�ӦʽΪVO2+-e-+H2O=VO2++2H+ |
| C�����ܵ��a��b������ĵ������Һ��ͨ�����ӵĶ����ƶ��γɱպϻ�· |
| D���ŵ�ʱ����ת�Ƶĵ�����Ϊ6.02��1023ʱ������1.0 mol H+���Ҳ�Ǩ�ƽ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������£���pH=3�Ĵ�����Һϡ�͵�ԭ�����10������Һ��pH=4 |
| B����0.2000mol/L NaOH����Һ�ζ�HCl��CH3COOH�Ļ����Һ�����Һ�����ֵ�Ũ�Ⱦ�ԼΪ0.1mol/L����������ʱ����Һ�е���δ����ȫ�к� |
| C��Ϊȷ��ij��H2A��ǿ�ỹ�����ᣬ�ɲ�NaHA��Һ��pH����pH��7����H2A�����ᣬ��pH��7����H2A��ǿ�� |
| D����ͬ�¶��£��������Ȼ�������ֱ������ͬ����Ģ�����ˮ����0.1mol?L���ᡢ��0.1mol/L�Ȼ�þ��Һ����0.1mol/L��������Һ�У�Ag+Ũ�ȣ��٣��ܣ��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ijѧ����һ�ο����������һ�����ڱ�д���֡���Ȥζʵ�飮��ֽ�����Ȼ��ơ���ɫ��̪�Ļ��Һ��ʪ��Ȼ��ƽ����һ�鲬Ƭ�ϣ���ͨ��Դ����Ǧ������ֽ��д�֣�����ֺ�ɫ�ּ����ݴˣ�����������ȷ���ǣ�������
ijѧ����һ�ο����������һ�����ڱ�д���֡���Ȥζʵ�飮��ֽ�����Ȼ��ơ���ɫ��̪�Ļ��Һ��ʪ��Ȼ��ƽ����һ�鲬Ƭ�ϣ���ͨ��Դ����Ǧ������ֽ��д�֣�����ֺ�ɫ�ּ����ݴˣ�����������ȷ���ǣ�������| A����Ƭ��������������������Ӧ |
| B��Ǧ�ʶ���������������ԭ��Ӧ |
| C��Ǧ�ʶ����������������� |
| D��a����������b���Ǹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCO3-ˮ������ӷ���ʽ��HCO3-+H2O�TCO32-+H3O+ | ||
| B��Ư����Һ�ڿ�����ʧЧ��ClO-+CO2+H2O=HClO+HCO3- | ||
| C��������SO2ͨ��NaOH��Һ�У�SO2-+2OH-=SO32-+H2O | ||
D������������ͭ����ȩ��Ӧ��CH3CHO+2Cu��OH��2+OH-
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��K+��Na+��Cl-��CO32- |
| B��Cu2+��Cl-��Na+��SO42- |
| C��Ca2+��Na+��Cl-��NO3- |
| D��Na+��Ag+��NO3-��Cl- |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com