
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 2:1 |
分析 镁铝合金粉末溶于足量盐酸中,加入过量NaOH 溶液,沉淀为氢氧化镁,则经洗涤、干燥、灼烧,得到白色粉末为氧化镁,氧化镁质量等于合金的质量,由组成可知氧化镁中氧元素的质量等于合金中铝的质量,以此来解答.
解答 解:由镁铝合金粉末溶于足量盐酸中,加入过量NaOH 溶液,沉淀为氢氧化镁,则经洗涤、干燥、灼烧,得到白色粉末为MgO,MgOg质量等于Mg、Al合金的质量,由组成可知氧化镁中氧元素的质量等于合金中铝的质量,则合金中Mg、Al的质量比为24:16=3:2,
故选A.
点评 本题考查混合物的计算,为高频考点,把握白色粉末为MgO及物质的组成为解答的关键,侧重分析与计算能力的考查,注意Mg元素的质量守恒,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:选择题
| A. | 胶体是一种液态混合物,属于分散系的一种 | |
| B. | 用丁达尔效应可区分Fe(OH)3胶体、水、CuSO4溶液 | |
| C. | 用过滤器可以将胶体和溶液分开 | |
| D. | 胶体的本质特征是发生丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口倒出 | |
| B. | 使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干 | |
| C. | 与金属反应时,稀HNO3被还原为NO,而浓HNO3被还原为NO2,故稀硝酸的氧化性强于浓硝酸 | |
| D. | 用10 mL量筒量取9.2 mL NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2 (g)+NaOH (aq)═NaHCO3 (aq)△H=-(2y-x)kJ/mol | |
| B. | CO2 (g)+NaOH (aq)═NaHCO3 (aq)△H=-(2x-y)kJ/mol | |
| C. | CO2 (g)+NaOH (aq)═NaHCO3 (aq)△H=-(4x-y)kJ/mol | |
| D. | 2CO2 (g)+2NaOH (1)═2NaHCO3 (1)△H=-(8x-2y)kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙酸的分子式:CH3COOH | B. | 甲烷的结构简式:CH4 | ||
| C. | 35Cl表示该氯原子核内有20个中子 | D. | SiO2是二氧化硅的分子式 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m>n | B. | m<n | C. | m=n | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
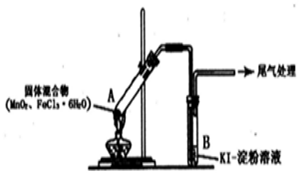
| 实验编号 | 操作 | 现象 |
| 实验1 | 按上图所示加热MnO2与FeCl3•6H2O 混合物 | ①试管A中部分固体溶解,上方出现白雾 ②稍后,产生黄色气体,管壁附着黄色液滴 ③试管B中溶液变蓝 |
| 实验2 | 把A中的混合物换为FeC13•6H2O,B中溶液换为KSCN溶液,加热. | A中部分固体溶解,产生白雾和黄色气体,B中KSCN溶液变红 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com