
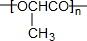 .
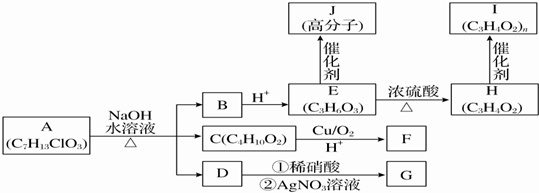
.分析 据A的分子式和在NaOH溶液中反应生成B酸化后的E的分子式可知,E中含有羟基和羧基,据A的分子式和在NaOH溶液中反应生成C的分子式可知,C为饱和二元醇,D能够与硝酸银溶液反应生成白色沉淀,可知D为NaCl,则A为含有Cl原子的酯,在NaOH溶液中发生卤代烃的水解和酯的水解,据E分子中含有一个连有4个不同原子或原子团的碳原子可知,E为CH3CHOHCOOH,B为CH3CHOHCOONa,据C分子中核磁共振氢谱中显示有四种不同的氢原子,且峰面积之比为4:3:2:1可知,C为CH2OHCH(CH3)CH2OH,则A为CH3CHClCOOCH2CH(CH3)CH2OH,E为CH3CHOHCOOH,能够通过酯化反应生成高分子化合物J,J为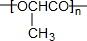 ,E在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,H通过加聚反应生成I,I为
,E在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,H通过加聚反应生成I,I为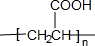 ,C为CH2OHCH(CH3)CH2OH,在Cu作催化剂时,催化氧化生成F,1mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2mol红色沉淀,F为OHCCH(CH3)CHO,据此分析.
,C为CH2OHCH(CH3)CH2OH,在Cu作催化剂时,催化氧化生成F,1mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2mol红色沉淀,F为OHCCH(CH3)CHO,据此分析.
解答 解:据A的分子式和在NaOH溶液中反应生成B酸化后的E的分子式可知,E中含有羟基和羧基,据A的分子式和在NaOH溶液中反应生成C的分子式可知,C为饱和二元醇,D能够与硝酸银溶液反应生成白色沉淀,可知D为NaCl,则A为含有Cl原子的酯,在NaOH溶液中发生卤代烃的水解和酯的水解,据E分子中含有一个连有4个不同原子或原子团的碳原子可知,E为CH3CHOHCOOH,B为CH3CHOHCOONa,据C分子中核磁共振氢谱中显示有四种不同的氢原子,且峰面积之比为4:3:2:1可知,C为CH2OHCH(CH3)CH2OH,则A为CH3CHClCOOCH2CH(CH3)CH2OH,E为CH3CHOHCOOH,能够通过酯化反应生成高分子化合物J,J为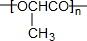 ,E在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,H通过加聚反应生成I,I为
,E在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,H通过加聚反应生成I,I为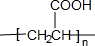 ,C为CH2OHCH(CH3)CH2OH,在Cu作催化剂时,催化氧化生成F,1mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2mol红色沉淀,F为OHCCH(CH3)CHO,
,C为CH2OHCH(CH3)CH2OH,在Cu作催化剂时,催化氧化生成F,1mol F与足量的新制氢氧化铜在加热条件下充分反应可生成2mol红色沉淀,F为OHCCH(CH3)CHO,
(1)A为CH3CHClCOOCH2CH(CH3)CH2OH,其中含氧官能团有酯基、羟基,故答案为:酯基、羟基;
(2)据上述分析,B为CH3CHOHCOONa,故答案为:CH3CHOHCOONa;
(3)E为CH3CHOHCOOH,在浓硫酸作用下发生消去反应生成H,H为CH2=CHCOOH,反应方程式为:CH3CHOHCOOH$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O,
故答案为:CH3CHOHCOOH$→_{△}^{浓硫酸}$CH2=CHCOOH+H2O;消去反应;
(4)D能够与硝酸银溶液反应生成白色沉淀,可知D为NaCl,故答案为:氯化钠;
(5)E为CH3CHOHCOOH,能够通过酯化反应生成高分子化合物J,J为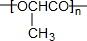 ,故答案为:
,故答案为: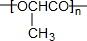 ;
;
(6)C为CH2OHCH(CH3)CH2OH,与C具有相同的官能团和相同的官能团数目,且官能团不在同一个碳原子上的C的同分异构体有:CH2OHCH2CH2CH2OH,CH2OHCHOHCH2CH3,CH2OHCH2CHOHCH3,CH3CHOHCHOHCH3,CH2OHC(CH3)OHCH3,共5种,其中核磁共振氢谱有三种不同化学环境的氢原子,且峰面积之比为2:2:1的是CH2OHCH2CH2CH2OH,故答案为:5;CH2OHCH2CH2CH2OH.
点评 本题考查有机物的推断,对学生的逻辑推理有较高的要求,注意掌握官能团的性质与转化,利用顺推法与逆推法结合进行推断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | c>d>a>b | B. | a>b>d>c | C. | b>a>d>c | D. | b>a>c>d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则转移4NA个电子 | |
| B. | 17.4 g某硫化磷(如图)中含P-S键数目为0.6NA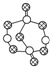 | |
| C. | 1 mol含8个碳原子的某烃分子,最多形成7 mol碳碳单键 | |
| D. | 标准状况下,22.4 L SO2与O2混合气体,含有2NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4熔化时,离子键和共价键均被破坏 | |
| B. | 过氧化氢中只有非极性共价键 | |
| C. | 金属元素与非金属元素化合时,一定形成离子键 | |
| D. | 非金属元素也可能形成离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com