
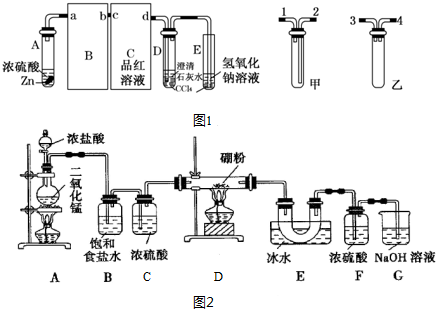
���� I����ʼC��D��E�о������ݲ�����������������٣�C��Ʒ����Һ��ɫ��D���ȳ��ֻ��Ǻ������ʧ��˵����ʼ��Ӧ���ɶ������÷�Ӧ֤��Ũ�������ǿ�����ԣ�D�ж������������������Ʒ�Ӧ����������Ƴ�������������������������ˮ��Ӧ������������ƣ������ܽ⣻�淴Ӧ����Ũ�����Ϊϡ���ᣬϡ������Zn��Ӧ��������������Ӧһ��ʱ���C��D��E�е��������ֻ��������ӣ��������ɵĶ���������C�о�������Ӧ������װ��������ѹǿ��С��Bװ�õ�����Ӧ�Ƿ�ֹ������ѡ���װ�ã�CҲѡ���װ��ʢ��Ʒ����Һ��E��������������δ��Ӧ�Ķ�������ֹ��Ⱦ������D��E�е��ܾ��������Ȼ�̼�У����Է�ֹ��Һ������
��Aװ���Ʊ�������������ӦΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����Bװ�����������л��е�HCl��C��Ũ������ˮ������������
��1��Aװ���Ʊ�����������������Ũ���ᷴӦ�����Ȼ��̡�������ˮ��
��2��BCl3�ķе�Ϊ12.5�棬�ӷ���Ӧ��ȴ�ռ���B���ڳ�ȥHCl���壬������ܻᷢ����Ӧ��2B+6HCl$\frac{\underline{\;\;��\;\;}}{\;}$2BCl3��+3H2������D�м��������������Ļ�����壬������ը��
��3��Fװ����������ˮ����������Gװ���е�ˮ��������U�ιܣ�Gװ��ʢװ����������Һ����β�����Դ��жϣ�
��4�����Ȼ�����ˮ���ҷ�Ӧ�������ᣨH3BO3���Ͱ���������������˵����HCl���ɣ���ʵ���ұ������Ȼ����ע������Ҫ�ܷⱣ�棬��ֹ�ܳ�ˮ�⣮
��� �⣺I����ʼC��D��E�о������ݲ�����������������٣�Ʒ����Һ��ɫ��D���ȳ��ֻ��Ǻ������ʧ��˵����ʼ��Ӧ���ɶ������÷�Ӧ֤��Ũ�������ǿ�����ԣ�D�ж������������������Ʒ�Ӧ����������Ƴ�������������������������ˮ��Ӧ������������ƣ������ܽ⣻�淴Ӧ����Ũ�����Ϊϡ���ᣬϡ������Zn��Ӧ��������������Ӧһ��ʱ���C��D��E�е��������ֻ��������ӣ��������ɵĶ���������C�о�������Ӧ������װ��������ѹǿ��С��Bװ�õ�����Ӧ�Ƿ�ֹ������ѡ���װ�ã�CҲѡ���װ��ʢ��Ʒ����Һ��E��������������δ��Ӧ�Ķ�������ֹ��Ⱦ������D��E�е��ܾ��������Ȼ�̼�У����Է�ֹ��Һ������
��1��������������֪����ȷ����˳��Ϊ��a��2��1��b��c��2��1��d��������1��2 ������D��E��֧�Թ���CCl4�������ǣ���ֹ������
�ʴ�Ϊ��2��1��2��1����ֹ��������
��2����֤��Ũ�������ǿ�����ԵĻ�ѧ����ʽΪ��Zn+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ZnSO4+SO2��+2H2O��
�ʴ�Ϊ��Zn+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ZnSO4+SO2��+2H2O��
��3����Ӧһ��ʱ�������Ũ����Ũ�Ƚ��ͣ�Zn��ϡ���ᷴӦ��H2���ɣ���Ӧһ��ʱ����������ֻ��������ӣ�
�ʴ�Ϊ����Ӧһ��ʱ�������Ũ����Ũ�Ƚ��ͣ�Zn��ϡ���ᷴӦ��H2���ɣ�
��4��D�л�����ʧ�����ӷ���ʽΪ��CaSO3+SO2+H2O�TCa2++2HSO3-��
�ʴ�Ϊ��CaSO3+SO2+H2O�TCa2++2HSO3-��
��1��Aװ���Ʊ�����������������Ũ���ᷴӦ�����Ȼ��̡�������ˮ����Ӧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2����
��2�����Ȼ���ķе�ͣ��ӷ�����Ҫ��ȴ��Ʒ��Eװ�õ������ǣ���ȴ���ռ����Ȼ���
Bװ�õ�����������Cl2�л��е�HCl������ȥBװ�ã����������֪�������Ȼ��ⷴӦ���ɵIJ����������������������������Ļ�����壬������ը��
�ʴ�Ϊ����ȴ���ռ����Ȼ���������Ȼ��ⷴӦ���ɵIJ����������������������������Ļ�����壬������ը��
��3��Fװ����������ˮ����������Gװ���е�ˮ��������U�ιܣ�Gװ����ʢװ����������Һ����β������ʵ���п�����һ��ʢװ��ʯ�ҵĸ����������F+Gװ�ã�
�ʴ�Ϊ����ʯ�ң�
��4�����Ȼ�����ˮ���ҷ�Ӧ�������ᣨH3BO3���Ͱ���������������˵����HCl���ɣ����Ȼ�����ˮ�ܷ�Ӧ�Ļ�ѧ����ʽΪ��BCl3+3H2O=H3BO3+3HCl������ʵ����Ӧ�ܷ��䰵���������Ȼ���
�ʴ�Ϊ��BCl3+3H2O�TH3BO3+3HCl�����ܷⱣ�森
���� ��ʵ�����������Ʊ�������ۺ����ʵ�飬������ѧ���ķ���������ʵ�������Ŀ��飬��Ŀ�漰�Ʊ����塢�������塢���������β����������ȷԭ���ǽ���ؼ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 0.1 mol•L-1NaHCO3��Һ��c��Na+����c��HCO3-����c��CO32-����c��H2CO3�� | |
| B�� | 0.1 mol•L-1NaHCO3��Һ��0.1 mol•L-1NaOH��Һ�������ϣ�c��Na+��=2c��CO32-��+c��HCO3-��+2c��H2CO3�� | |
| C�� | 0.1 mol•L-1NaHCO3��Һ��0.2 mol•L-1NaOH��Һ�������ϣ�c��Na+����c��OH-����0.05 mol•L-1��c��CO32-����c��HCO3-�� | |
| D�� | 0.2 mol•L-1NaHCO3��Һ��0.1 mol•L-1NaOH��Һ�������ϣ�c��CO32-��+2c��OH-��=c��HCO3-��+3c��H2CO3��+2c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
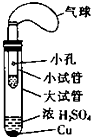 ijͬѧ�������ͼ��ʾ����ʵ��װ�ã�����װ��δ���������Ʊ�SO2������ʵ�������������仹ԭ�ԣ��Ʊ�SO2ʱѡ�õ��Լ�ΪCu��ŨH2SO4���ش��������⣺
ijͬѧ�������ͼ��ʾ����ʵ��װ�ã�����װ��δ���������Ʊ�SO2������ʵ�������������仹ԭ�ԣ��Ʊ�SO2ʱѡ�õ��Լ�ΪCu��ŨH2SO4���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ���ӵ���������������غ� | B�� | ����������������IJ��غ� | ||
| C�� | H2O2�Ǽ��Է��� | D�� | H2O2�ǷǼ��Է��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ʵ������һƿ�����Ȼ��Ƶ��������ƹ����Լ������ⶨ�������Ƶ���������ԼΪ82%��Ϊ����֤�䴿�ȣ���Ũ��Ϊ0.2mol•L-1��������еζ�������������⣺
ʵ������һƿ�����Ȼ��Ƶ��������ƹ����Լ������ⶨ�������Ƶ���������ԼΪ82%��Ϊ����֤�䴿�ȣ���Ũ��Ϊ0.2mol•L-1��������еζ�������������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 11.2 LO2��O3��ɵĻ�����庬��ԭ����ΪNA | |
| B�� | ���³�ѹ�£�1.7 g NH3���еĵ�����ĿΪ NA | |
| C�� | 0.1mol/LNa2SO4��Һ�к���Na+�ĸ���Ϊ0.2NA | |
| D�� | ��״���£�22.4 L NO2��������H2O��ַ�Ӧ��ת�Ƶ�����Ϊ NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��һ�δ�ĥ����þ������������ˮ�� | |
| B�� | ��Cl2ͨ��FeCl2��Һ�� | |
| C�� | ���̶���ļ�Ͷ�뵽ˮ�� | |
| D�� | ����ˮ�μӵ�KI������Һ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com