
 CO2(g) + H2(g);1molCO完全反应放热a kJ。反应达到平衡后,测得n(CO2)= 0.8mol下列说法正确的是( )
CO2(g) + H2(g);1molCO完全反应放热a kJ。反应达到平衡后,测得n(CO2)= 0.8mol下列说法正确的是( )| A.判断该反应达到平衡的依据是CO、H2O、CO2、H2的浓度都相等 |
| B.反应放出的热量为0.4a kJ |
| C.平衡时H2O 的转化率为40% |
| D.加入催化剂可以反应加快,放热更多 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题
 CO(g) + H2(g)反应,一定条件下达到平衡,①增大水蒸汽浓度,平衡向 反应方向移动(填“正”、“逆”或“不”下同),CO的浓度将 。(填“增大”、“减小”或“不变”下同)
CO(g) + H2(g)反应,一定条件下达到平衡,①增大水蒸汽浓度,平衡向 反应方向移动(填“正”、“逆”或“不”下同),CO的浓度将 。(填“增大”、“减小”或“不变”下同) N2O4(g) 当活塞迅速向外拉时,平衡向 反应方向移动,气体的颜色先变_____(“浅”、“深”或“不变”下同),后变______;最终和最初相比,_____更深(填“前”或“后”)。
N2O4(g) 当活塞迅速向外拉时,平衡向 反应方向移动,气体的颜色先变_____(“浅”、“深”或“不变”下同),后变______;最终和最初相比,_____更深(填“前”或“后”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 物质 | O2 | S | Se | Te |
| ΔH(kJ·mol-1) | -242 | -20 | 81 | |
 (填“一定增大”、“一定减小”或“不能确定”)。
(填“一定增大”、“一定减小”或“不能确定”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:判断题

 XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。
XeF4(g)+F2(g),其反应热ΔH0(填“>”“=”或“<”=。理由是__________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 FeO(s) + CO(g),其温度与平衡常数K的关系如下表:
FeO(s) + CO(g),其温度与平衡常数K的关系如下表:| T(K) | 938 | 1173 |
| K | 1.47 | 2.15 |
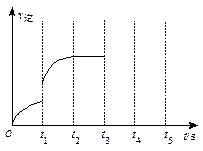
 画出t3~ t5时间段的v逆变化曲线。
画出t3~ t5时间段的v逆变化曲线。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是 | A.容器内压强不随时间变化 | B.容器内密度不随时间变化 |
| C.容器内X、Y、Z的浓度之比为1︰2︰2 | |
| D.单位时间消耗0.1 mol X同时生成0.2 mol Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.当一个可逆反应达到化学平衡状态时,正向反应速率和逆向反应速率都等于零 |
| B.一个可逆反应达到的平衡状态就是这个反应在该条件下所能达到的限度 |
| C.化学平衡状态时,各物质的浓度保持相等 |
| D.化学反应的限度由反应物的本性决定,是不可改变的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2AB(g)达到平衡状态的标志是( )
2AB(g)达到平衡状态的标志是( )| A.单位时间内生成n molA2,同时生成n molAB |
| B.容器内混合气体的平均相对分子质量不随时间变化 |
| C.单位时间内生成2n molAB,同时生成n molB2 |
| D.单位时间内一个A-A键断裂,同时生成二个A-B键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com