
‘Ύ“ΜΟή±’ΒΡ»ίΤς÷–Θ§”…“ΜΕ®ΝΩΒΡA4(s)ΚΆB2(g)Ζ¥”ΠΘ§Ω…ΒΟΒΫAB5(g)ΚΆAB3(g)Εΰ÷÷≤ζΈοΘ§…ζ≥…Έο‘ΎΗςΗωΈ¬Ε»œ¬ΒΡΤΫΚβ≈®Ε»c”κΈ¬Ε»TΒΡΙΊœΒ»γΆΦΓΘœ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ® Θ©
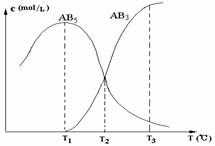
AΘ°AB5(g)![]() AB3(g)ΘΪB2(g)ΤδΖ¥”ΠΒΡΖ¥”Π»»ΠΛHΘΨ0
AB3(g)ΘΪB2(g)ΤδΖ¥”ΠΒΡΖ¥”Π»»ΠΛHΘΨ0
BΘ°A4(s)ΘΪ10B2(g) ![]() 4AB5(g) ΤδΖ¥”ΠΒΡΖ¥”Π»»ΠΛHΘΦ0
4AB5(g) ΤδΖ¥”ΠΒΡΖ¥”Π»»ΠΛHΘΦ0
CΘ°‘ΎT2 ±ΩΧΘ§±Θ≥÷Έ¬Ε»≤Μ±δΘ§ΗχΧεœΒΦ”―ΙΘ§¥οΒΫ–¬ΤΫΚβ ±Θ§n(AB5)ΘΨn(AB3)
DΘ°‘ΎT1ΓΔT2ΓΔT3 ±Θ§»ίΤς÷–B2ΒΡΈο÷ ΒΡΝΩΒΡ¥σ–ΓΙΊœΒΈΣn(B2,T3)ΘΨn(B2,T2)ΘΨn(B2,T1)
 –Γ―ßΫΧ≤ΡΆξ»ΪΫβΕΝœΒΝ–¥πΑΗ
–Γ―ßΫΧ≤ΡΆξ»ΪΫβΕΝœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
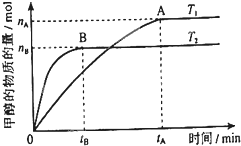 ΩΤ―ßΦ“άϊ”ΟΧΪ―τΡήΖ÷ΫβΥ°…ζ≥…ΒΡ«βΤχ‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬”κΕΰ―θΜ·ΧΦΖ¥”Π…ζ≥…ΦΉ¥ΦΘ§≤ΔΩΣΖΔ≥ω÷±Ϋ”“‘ΦΉ¥ΦΈΣ»ΦΝœΒΡ»ΦΝœΒγ≥ΊΘ°“―÷ΣH2Θ®gΘ©ΓΔCOΘ®gΘ©ΚΆCH3OHΘ®lΘ©ΒΡ»Φ…’»»ΓςHΖ÷±πΈΣ-285.8kJ?mol-1ΓΔ-283.0kJ?mol-1ΚΆ-726.5kJ?mol-1Θ°«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΩΤ―ßΦ“άϊ”ΟΧΪ―τΡήΖ÷ΫβΥ°…ζ≥…ΒΡ«βΤχ‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬”κΕΰ―θΜ·ΧΦΖ¥”Π…ζ≥…ΦΉ¥ΦΘ§≤ΔΩΣΖΔ≥ω÷±Ϋ”“‘ΦΉ¥ΦΈΣ»ΦΝœΒΡ»ΦΝœΒγ≥ΊΘ°“―÷ΣH2Θ®gΘ©ΓΔCOΘ®gΘ©ΚΆCH3OHΘ®lΘ©ΒΡ»Φ…’»»ΓςHΖ÷±πΈΣ-285.8kJ?mol-1ΓΔ-283.0kJ?mol-1ΚΆ-726.5kJ?mol-1Θ°«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ| nA |
| tA |
| 2-a |
| 2 |
| 2-a |
| 2 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
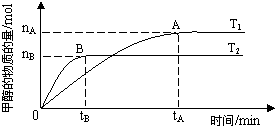 ΩΤ―ßΦ“άϊ”ΟΧΪ―τΡήΖ÷ΫβΥ°…ζ≥…ΒΡ«βΤχ‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬”κΕΰ―θΜ·ΧΦΖ¥”Π…ζ≥…ΦΉ¥ΦΘ§≤ΔΩΣΖΔ≥ω÷±Ϋ”“‘ΦΉ¥ΦΈΣ»ΦΝœΒΡ»ΦΝœΒγ≥ΊΘ°“―÷ΣH2Θ®gΘ©ΓΔCOΘ®gΘ©ΚΆCH3OHΘ®lΘ©ΒΡ»Φ…’»»ΓςHΖ÷±πΈΣ-285.8kJ?mol-1ΓΔ-283.0kJ?mol-1ΚΆ-726.5kJ?mol-1Θ°
ΩΤ―ßΦ“άϊ”ΟΧΪ―τΡήΖ÷ΫβΥ°…ζ≥…ΒΡ«βΤχ‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬”κΕΰ―θΜ·ΧΦΖ¥”Π…ζ≥…ΦΉ¥ΦΘ§≤ΔΩΣΖΔ≥ω÷±Ϋ”“‘ΦΉ¥ΦΈΣ»ΦΝœΒΡ»ΦΝœΒγ≥ΊΘ°“―÷ΣH2Θ®gΘ©ΓΔCOΘ®gΘ©ΚΆCH3OHΘ®lΘ©ΒΡ»Φ…’»»ΓςHΖ÷±πΈΣ-285.8kJ?mol-1ΓΔ-283.0kJ?mol-1ΚΆ-726.5kJ?mol-1Θ°| nA |
| tA |
| n(H2) |
| n(CH3OH) |
| 2-a |
| 2 |
| 2-a |
| 2 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
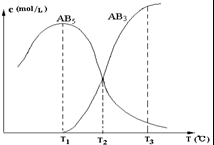 ‘Ύ“ΜΟή±’ΒΡ»ίΤς÷–Θ§”…“ΜΕ®ΝΩΒΡA4Θ®sΘ©ΚΆB2Θ®gΘ©Ζ¥”ΠΘ§Ω…ΒΟΒΫAB5Θ®gΘ©ΚΆAB3Θ®gΘ©Εΰ÷÷≤ζΈοΘ§…ζ≥…Έο‘ΎΗςΗωΈ¬Ε»œ¬ΒΡΤΫΚβ≈®Ε»c”κΈ¬Ε»TΒΡΙΊœΒ»γΆΦΘ°œ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ®ΓΓΓΓΘ©
‘Ύ“ΜΟή±’ΒΡ»ίΤς÷–Θ§”…“ΜΕ®ΝΩΒΡA4Θ®sΘ©ΚΆB2Θ®gΘ©Ζ¥”ΠΘ§Ω…ΒΟΒΫAB5Θ®gΘ©ΚΆAB3Θ®gΘ©Εΰ÷÷≤ζΈοΘ§…ζ≥…Έο‘ΎΗςΗωΈ¬Ε»œ¬ΒΡΤΫΚβ≈®Ε»c”κΈ¬Ε»TΒΡΙΊœΒ»γΆΦΘ°œ¬Ν–ΥΒΖ®¥μΈσΒΡ «Θ®ΓΓΓΓΘ©| AΓΔAB5Θ®gΘ©?AB3Θ®gΘ©+B2Θ®gΘ©ΤδΖ¥”ΠΒΡΖ¥”Π»»ΓςHΘΨ0 | BΓΔA4Θ®sΘ©+10B2Θ®gΘ©?4AB5Θ®gΘ©ΤδΖ¥”ΠΒΡΖ¥”Π»»ΓςHΘΦ0 | CΓΔ‘ΎT2 ±ΩΧΘ§±Θ≥÷Έ¬Ε»≤Μ±δΘ§ΗχΧεœΒΦ”―ΙΘ§¥οΒΫ–¬ΤΫΚβ ±Θ§nΘ®AB5Θ©ΘΨnΘ®AB3Θ© | DΓΔ‘ΎT1ΓΔT2ΓΔT3 ±Θ§»ίΤς÷–B2ΒΡΈο÷ ΒΡΝΩΒΡ¥σ–ΓΙΊœΒΈΣnΘ®B2Θ§T3Θ©ΘΨnΘ®B2Θ§T2Θ©ΘΨnΘ®B2Θ§T1Θ© |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ≥±÷ί –2008ΡξΗΏΩΦΒΎΕΰ¥ΈΡΘΡβ≤β ‘ΓΔΜ·―ß ‘Χβ Χβ–ΆΘΚ021
|
‘Ύ“ΜΟή±’ΒΡ»ίΤς÷–Θ§”…“ΜΕ®ΝΩΒΡA4(s)ΚΆB2(g)Ζ¥”ΠΘ§Ω…ΒΟΒΫAB5(g)ΚΆAB3(g)Εΰ÷÷≤ζΈοΘ§…ζ≥…Έο‘ΎΗςΗωΈ¬Ε»œ¬ΒΡΤΫΚβ≈®Ε»c”κΈ¬Ε»TΒΡΙΊœΒ»γΆΦΘ°œ¬Ν–ΥΒΖ®¥μΈσΒΡ «
| |
AΘ° |
AB5(g) |
BΘ° |
A4(s)ΘΪ10B2(g) |
CΘ° |
‘ΎT2 ±ΩΧΘ§±Θ≥÷Έ¬Ε»≤Μ±δΘ§ΗχΧεœΒΦ”―ΙΘ§¥οΒΫ–¬ΤΫΚβ ±Θ§n(AB5)ΘΨn(AB3) |
DΘ° |
‘ΎT1ΓΔT2ΓΔT3 ±Θ§»ίΤς÷–B2ΒΡΈο÷ ΒΡΝΩΒΡ¥σ–ΓΙΊœΒΈΣn(B2Θ§T3)ΘΨn(B2Θ§T2)ΘΨn(B2Θ§T1) |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com