
将0.2 mol·L-1 HCOOH溶液加水稀释,下列说法正确的是( )
A.溶液中c(H+)和c(OH-)都减小 B.溶液中c(H+)增大
C.醋酸电离平衡向左移动 D.溶液的pH增大
科目:高中化学 来源:2015-2016学年陕西省高一上学期期中测试化学试卷(解析版) 题型:填空题
选择下列实验方法分离物质,将合理的分离方法的字母填在横线上。
A 萃取分液 B 加热分解 C 结晶 D 分液 E 蒸馏 F 过滤
(1)________分离饱和食盐水和沙子的混合物
(2)________从硝酸钾和氯化钠的混合溶液中获得硝酸钾
(3)________分离水和苯的混合物
(4)________分离四氯化碳(沸点为76.75 ℃)和甲苯(沸点为110.6 ℃)的混合物
(5)在“粗盐提纯”的实验中,多次用到玻璃棒,在溶解、过滤、蒸发三个步骤中,玻璃棒所起的作用分别是 ; ;________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省金兰教育合作组织高一上学期期中联考化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.同温同压下,相同体积的物质,它们的物质的量必相等
B.任何条件下,等物质的量的N2和CO所含的分子数必相等
C.1L一氧化碳气体一定比1L氧气的质量小
D.铁的摩尔质量在数值上等于铁原子的相对原子质量
查看答案和解析>>
科目:高中化学 来源:2016届广东省惠州市高三上学期第二次调研测试化学试卷(解析版) 题型:选择题
2015年诺贝尔生理学或医学奖授予我国女药学家屠呦呦,她从中药中分离出青蒿素应用于疟疾治疗。青蒿素的键-线结构简式如图。下列关于青蒿素的说法不正确的是

A.分子式为C15H22O5青蒿素(键线式)
B.属于芳香族化合物
C.可发生水解反应
D.含有过氧键(-O-O-)有强氧化性
查看答案和解析>>
科目:高中化学 来源:2016届山东省高三上学期12月阶段测化学试卷(解析版) 题型:选择题
下列关于药品的使用和保存,仪器选用正确的是
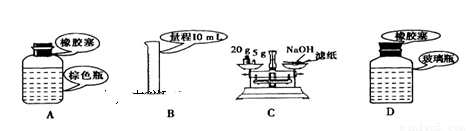
A.实验室中保存浓硝酸 B.准确量取9.50 mL稀硫酸
C.用托盘天平称量NaOH固体 D.实验室中保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
有一种军用烟幕弹中装有ZnO、Al粉和C2Cl6,其发烟过程中的化学反应如下:
①3ZnO+2Al=Al2O3+3Zn;②3Zn+C2Cl6=3ZnCl2+2C。
下列有关叙述不正确的是( )
A.反应①是铝热反应 B.反应②是置换反应
C.C2Cl6属于有机物 D.烟幕是小液滴分散在空气中形成的
查看答案和解析>>
科目:高中化学 来源:2016届广东省七校联合体高三上学期第二次联考理综化学试卷(解析版) 题型:填空题
硫酸法是现代氧化铍或氢氧化铍生产中广泛应用的方法之一, 其原理是利用预焙烧破坏铍矿物(绿柱石—3BeO· Al2O3·6SiO2及少量FeO等)的结构与晶型, 再采用硫酸酸解含铍矿物, 使铍、铝、铁等酸溶性金属进入溶液相, 与硅等脉石矿物初步分离, 然后将含铍溶液进行净化、除杂, 最终得到合格的氧化铍( 或氢氧化铍) 产品, 其工艺流程如右图。
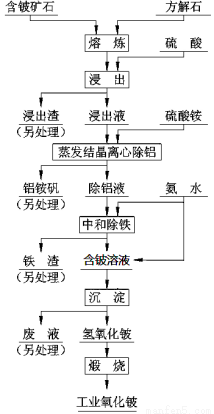
已知:(1)铝铵矾的化学式是NH4Al(SO4)2·12H2O(2)铍元素的化学性质与铝元素相似
根据以上信息回答下列问题:
(1)熔炼物酸浸前通常要进行粉碎,其目的是: ;
(2)“蒸发结晶离心除铝”若在中学实验室中进行,完整的操作过程是_____________________洗涤、过滤。
(3)“中和除铁”过程中“中和”所发生反应的离子方程式是__________________,用平衡原理解释“除铁”的过程_____________________。
(4)加入的“熔剂”除了流程中的方解石外,还可以是纯碱、石灰等。其中, 石灰具有价格与环保优势, 焙烧时配料比( m石灰/ m绿柱石) 通常控制为1:3, 焙烧温度一般为1400℃—1500℃ 。若用纯碱作熔剂,SiO2与之反应的化学方程式是__________________________,若纯碱加入过多则Al2O3、BeO也会发生反应,其中BeO与之反应的化学方程式是_______________________,从而会导致酸浸时消耗更多硫酸,使生产成本升高,结合离子方程式回答成本升高的原因_____________________。
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春市高三上学期质检化学试卷(解析版) 题型:填空题
常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如图1处理方法回收废电池中的各种资源.
(1)填充物用60℃温水溶解,目的是 .
(2)操作A的名称为 .
(3)铜帽溶解时加入H2O2的目的是 (用化学方程式表示).铜帽溶解完全后,可采用 方法除去溶液中过量的H2O2.
(4)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为 .
(5)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4=3MnSO4+4CO2↑+6H2O.
①当1mol MnO2参加反应时,共有 mol电子发生转移.
②MnO(OH)与浓盐酸在加热条件下也可发生反应,试写出该应的化学方程式: .
(6)锌锰干电池所含的汞可用KMnO4溶液吸收.在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图2所示:
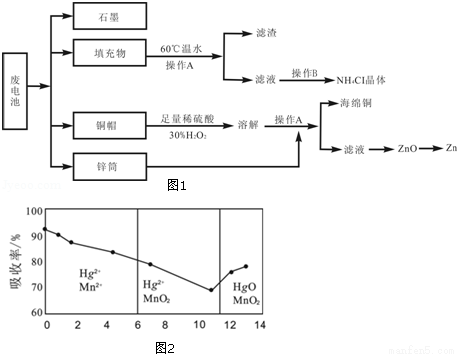
根据图可知:
①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率 .
②在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下 强.
查看答案和解析>>
科目:高中化学 来源:2016届四川省自贡市高三上第一次诊断考试理综化学试卷(解析版) 题型:选择题
下列环保建议中,你认为不能采纳的是
A.开发、使用新能源
B.废旧电池应集中回收,并填埋处理
C.用天然气代替汽油和柴油作发动机燃料
D.禁止将未经处理的工业废水和生活污水任意排放
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com