
| A、浓硫酸是一种干燥剂,能够干燥氢气、氧气、氨气等气体,但不能干燥有较强还原性的HI、H2S等气体 | ||||
B、浓硫酸与单质硫反应的方程式为:2H2SO4(浓)+S
| ||||
| C、把足量铜粉投入到只含H2SO4 2 mol的浓硫酸中,得到气体体积在标准状况下为22.4 L | ||||
| D、常温下能够用铁、铝等容器盛放浓H2SO4,是因为浓H2SO4的强氧化性使其钝化 |
| ||
| ||


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| 催化剂 |
| 点燃 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+ |
| B、Mg2+ |
| C、Fe2+ |
| D、A13+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2O |
| B、NO |
| C、NO2 |
| D、N2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
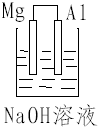 如图所示装置中:
如图所示装置中:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铜锌原电池中铜是负极 |
| B、铜银原电池中铜是正极 |
| C、用电解法精炼粗铜时,粗铜作阳极 |
| D、电解稀硫酸制H2、O2时,铜作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素A、B组成的化合物可能是NH3 |
| B、一定条件下,元素C、D的最高价氧化物对应的水化物之间不能发生反应 |
| C、C、D、E的半径:C>D>E |
| D、化合物AE与CE具有相同类型的化学键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com