
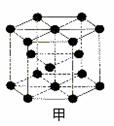
A��G��ǰ�����ڳ�ϡ������֮��ԭ�������������������Ԫ�ء�A������Ԫ�ؼȲ�ͬ�����ֲ�ͬ�壻B��C�ļ۵��Ӳ���δ�ɶԵ���������2��E�����s��p�ܼ��ĵ���������ȣ�F��Eͬ�����ҵ�һ�����ܱ�EС��G�ģ�1�����ӣ�G+���ĸ������ȫ������������Ŀ�ش��������⣺
��1��Ԫ��������B ��G ��
��2��F�ļ۵����Ų�ͼ ��
��3��д��������BC�Ľṹʽ ��
��4������[F(CA)4]�� ��F��ˮ��Һ�е�һ�ִ�����ʽ������F���ӻ������� ��
 |
��6��B��C֮���Ԫ��K������A�γ�KA3��G��������KA3���γ�[G(KA3)4]2+���ӣ�1mol[G(KA3)4]2+�����к��еĦҼ������ʵ���Ϊ mol��
��7���ڲⶨA��D�γɵķ��ӵ���Է�������ʱ��ʵ��ⶨֵһ���������ֵ����Ҫԭ���� ��
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
H2C2O4 (����)�Ƕ�Ԫ���ᣬKHC2O4��Һ�����ԡ���0.1mol��L-1 KHC2O4��Һ�У���ϵ��ȷ
����
A��c(K+)��c(H+)��c(HC2O4��)��c(OH��)��c(C2O42-) B��c(HC2O4��)��c(C2O42-)=0.1 mol��L -1
C��c(C2O42��)��c(H2C2O4) D��c(K+)��c(H2C2O4)��c(HC2O4��)��c(C2O42��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪1 g������ȫȼ������ˮ����ʱ�ų�����121 kJ.��1 mol ���������еĻ�ѧ����ȫ����ʱ��������496 kJ,ˮ������1 mol H�DO���γ�ʱ�ų�����463 kJ����������1mol H��H������ʱ��������Ϊ
A�� 920 kJ ��B�� 557 kJ ��C�� 436 kJ ��D�� 188 Kj
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵������ȷ���ǣ� ��
A.��Ϊͬ���칹��ķ��ӽṹ������ȫ��ͬ
B.������CH3-CH��NH2��-COOH���������칹��
C.��״���£���ͬ�����NH3 ��CH4 ��HF������ͬ�ĵ�����
D.�������CO��N2��Ϻ����õĻ�������ƽ��Ħ������Ϊ28 g/mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij������ʽΪC6H12O2 ������ˮ�������A��B��B��A��ͬ���칹��������������Ϊ�� �� ��
A��CH3CH(CH3)COOC2H5 B��CH3CH2COO(CH2)2CH3
C��CH3COO(CH2)3CH3 D��CH3CH2COOCH(CH3)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ��ѧ��Ҫ������ѧר�����������������йػ�ѧ������ȷ���ǣ� ��
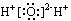 A��H2O�ĵ���ʽ�� B��������Ϊ14��̼ԭ�ӣ�
A��H2O�ĵ���ʽ�� B��������Ϊ14��̼ԭ�ӣ�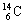
C��CO2�ı���ģ�ͣ� D��Cl���Ľṹʾ��ͼ��
D��Cl���Ľṹʾ��ͼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��д��ȷ���ǣ� ��
A��FeCl2��Һ��Cl2��Ӧ��2Fe2+ + Cl2 �T�T 2Fe3+ + 2Cl��
B��AlCl3��Һ�м��������İ�ˮ��Al3++ 3OH�� �T�T Al(OH)3��
C�����Ȼ�����Һ�м���ͭ�ۣ�Fe3+ + Cu �T�T Fe2+ + Cu2+
D������Ͷ�뵽NaOH��Һ�У�2Al + 2OH���T�T 2AlO2�� + H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ȥSO2�л��е�HC1���壬��ѡ�õ��Լ��� �� ��
A ʯ��ˮ BŨ���� C����NaHSO3��Һ D����Na2SO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������Ӱ뾶֮��С��1���ǣ� ����
A��r (Na+)/ r (Na) B��r (Cl-)/ r (Cl) C��r (Na)/ r (Mg) D��r (Ca)/ r (Mg)
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com