
【题目】下列各组气体通常条件下不能相互发生化学反应的是
A. SO2和H2S B. Cl2和CO2 C. H2和F2 D. NH3和HCl
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下的恒容容器中.当下列物理量不再发生变化时,不能表明反应:A(s)+3B(g)![]() 2C(g)+D(g)己达平衡状态的是( )
2C(g)+D(g)己达平衡状态的是( )
A. 混合气体的压强 B. 混合气体的密度
C. 3v逆(C)=2v正(B) D. 气体的平均相对分子质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(化学与技术)聚合氯化铝晶体的化学式为[Al2(OH)nCl6-n·xH2O]m,它是一种高效无机水处理剂,它的制备原理是调节增大AlCl3溶液的pH,通过促进其水解而结晶析出。其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:

(1)搅拌加热操作过程中发生反应的离子方程式 ;
(2)生产过程中操作B和D的名称均为 (B和D为简单操作)。
(3)反应中副产品a是 (用化学式表示)。
(4)生产过程中可循环使用的物质是 (用化学式表示)。
(5)调节pH至4.0~4.5的目的是 。
(6)实验室要测定水处理剂产品中n和x的值。为使测定结果更准确,需得到的晶体较纯净。生产过程中C物质可选用 。
A.NaOH | B.Al | C.氨水 | D.Al2O3E.NaAlO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、W、X、Y、Z是原子序数依次增大的短周期元素,Q和Y均满足主族序数与周期序数相等,Q与X、W与Z同主族,Q和W能形成原子个数之比为1:1和2:1的常见化合物。下列说法正确的是( )
A. 原子半径:Z>Y>X>W>Q
B. Q、X形成的化合物的电子式为![]()
C. 最简单氢化物的稳定性:Z>W
D. 工业上常用电解的方法制备X、Y的单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
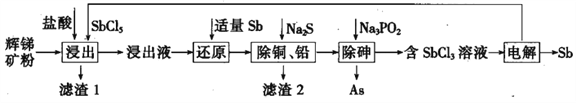
已知:① 浸出液中除含过量盐酸和SbCl5之外,还含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________(填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_________________。
(3)“还原”时,被Sb还原的物质为_____________(填化学式)。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于______;所加Na2S也不宜过多,其原因为_____________。
(5)“除砷”时有H3PO3生成,该反应的化学方程式为________________。
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_______。
(7)一种突破传统电池设计理念的镁-锑液态金属储能电池工作原理如图所示:

该电池由于密度的不同,在重力作用下分为三层,工作时中间层熔融盐的组成不变。充电时,C1-向_____(填“上”或“下”)移动;放电时,正极的电极反应式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有下列六组物质:属于同系物的是______,属于同分异构体是______,属于同种物质的是______。(填序号)
A.![]() 与
与![]() B.
B.![]() 与
与![]()
C.![]() 与
与![]() D.
D.![]() 与
与![]()
E.ClC(CH3)3与(CH3)2CHCH2Cl F.![]() 与CH3﹣CH2Cl.
与CH3﹣CH2Cl.
(2)![]() 的名称(系统命名法):_________________________;
的名称(系统命名法):_________________________;
(3)相对分子质量为72且沸点最低的烷烃的结构简式_________________________;
(4)工业生产TNT烈性炸药的化学方程式:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表是A、B、C三种烃的有关信息;
A | B | C |
①能使溴的四氯 化碳溶液褪色; ②比例模型为:
| ①平面型结构 ②棍模型为: | ①能使溴的四氯化碳溶液褪色; ②1mol能与2molH2在一定条件下反应 生成A ③比例模型为: |
图1 |
|
根据表中信息回答下列问题:
(1)如图1是烃B与液溴制取溴苯的装置,试回答:
(a)装置C中的现象___________________________________.
(b)装置B的作用__________________________________.
(2)如图2是制取烃C的装置,试回答:
(a)为了控制生成乙炔的速率,分液漏斗中盛放的液体是_______________。
(b)滴下液体后烧瓶中发生反应生成乙炔,写出此反应的化学方程式:_________。
(c)电石中含有硫化钙杂质,产生H2S,PH3等气体,为了不对乙炔性质造成干扰,应该除杂,一般选用___________洗气。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁是一种常见的水处理剂,无水氯化铁遇潮湿空气,极易吸水生成FeCl3nH2O。在实验室中,可以采用下列仪器和药品制取较纯的无水氯化铁固体。
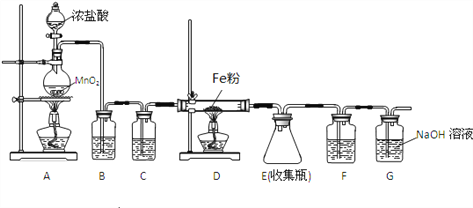
(1)实验开始时,先点燃____处的酒精灯(填A或D)。A中发生反应的化学方程式为____________________________________________。
(2)B装置中盛放的是饱和食盐水,其作用为__________________________________
(3)F装置中的试剂为浓硫酸,其作用是防止G中的水蒸气进入E中。用一件仪器装填适当试剂后,也可起到F和G的作用,所装填的试剂为_______________。
(4)G装置中反应的离子方程式为_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com