
1mol白磷转化为红磷时放出18.39kJ热量,已知:P4(白磷,s)+5O2(g)═2P2O5(s)△H=﹣a kJ/mol(a>0);4P(红磷,s)+5O2(g)═2P2O5(s)△H=﹣b kJ/mol(b>0),则a和b的关系是( )
|
| A. | a>b | B. | a=b | C. | a<b | D. | 无法确定 |
考点:
用盖斯定律进行有关反应热的计算.
专题:
化学反应中的能量变化.
分析:
根据已知热化学方程式,构造P4(白磷,s)=4P(红磷,s)△H=﹣18.39kJ/mol,根据△H与a、b的关系判断.
解答:
解:已知:①P4(白磷,s)+5O2(g)=2P2O5(s)△H=﹣a kJ/mol(a>0);
②4P(红磷,s)+5O2(g)=2P2O5(s)△H=﹣bkJ/mol(b>0),
根据盖斯定律可知,①﹣②即得到P4(白磷,s)=4P(红磷,s),
所以反应热△H=﹣a kJ/mol+bkJ/mol=﹣18.39kJ/mol,所以a大于b;
故选A.
点评:
考查盖斯定律、反应热的有关计算,难度不大,可以根据能量守恒定律进行判断.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
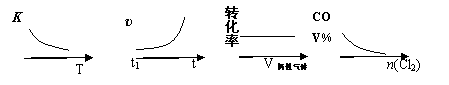
COCl2(g)  CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
① ② ③ ④
A.①表示随温度升高,平衡常数的变化
B.②表示加入催化剂,反应速率随时间的变化
C.③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D.④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红色
B.Al3+、NO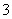 、Cl-、CO
、Cl-、CO 、Na+可大量共存于pH=2的溶液中
、Na+可大量共存于pH=2的溶液中
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列操作中,能使电离平衡H2O⇌H++OH﹣,向右移动且溶液呈酸性的是( )
|
| A. | 向水中加入NaHSO4溶液 | B. | 向水中加入Al2(SO4)3溶液 |
|
| C. | 向水中加入NaOH溶液 | D. | 将水加热到100℃,使pH=6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在温度压强不变时,1mol NO2高温分解,生成NO和O2,达到平衡时容器内气体的物质的量变为1.2mol,这时NO2的转化率为( )
|
| A. | 10% | B. | 20% | C. | 40% | D. | 50% |
查看答案和解析>>
科目:高中化学 来源: 题型:
请将下列物质的序号按要求填空:①石墨②铁钉③氧化钠④二氧化硫⑤水⑥盐酸⑦硫酸⑧氢氧化钙⑨氟化钠⑩甲烷,其中属于电解质的是 ,属于非电解质的是 ,属于强电解质的是 ,属于弱电解质的是 .写出③的电子式: ,⑩的结构式 ,⑨的水溶液显 (填“酸性”、“碱性”、“中性”),用离子方程式解释 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液蒸干后,能析出溶质固体的是( )
①FeCl3 ②Fe2(SO4)3 ③Ca(HCO3)2 ④Na2CO3.
|
| A. | 仅①④ | B. | 仅②④ | C. | 仅①② | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示2个甲分子反应生成1个丙分子和3个乙分子,下列判断不正确的是()

A. 1个乙分子中含有2个A原子
B. 摩尔质量关系为:2M (甲)=M (乙)+M (丙)
C. 该反应一定属于氧化还原反应
D. 该反应类型是分解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com