
”¾ĢāÄæ”æ£Ø1£©ŗܶąŗ¬ĀČĪļÖŹ¶¼ÄÜ×öĻū¶¾¼Į”£ŅŗĀČæÉŅŌÓĆÓŚŅūÓĆĖ®Ļū¶¾£¬µ«ŹĒĻū¶¾ŗóµÄĖ®ÖŠæÉÄܲśÉśĪ£ŗ¦ČĖĢ彔浵ÄÓŠ»śŃõ»ÆĪļ”£ŹĄ½ēø÷¹śĀ½ŠųæŖ·¢ŠĀŠĶ×ŌĄ“Ė®Ļū¶¾¼Į£¬ĻĀĮŠĪļÖŹæÉŅŌÓĆÓŚ×ŌĄ“Ė®Ļū¶¾µÄÓŠ___”£
A£®Na2O2 B£®Cl2O2 C£®O3 D£®O2 E£®ClO2
£Ø2£©Na2FeO4ĪŖ×ĻÉ«ĪļÖŹ£¬Ņ²æÉŅŌÓĆÓŚ×ŌĄ“Ė®Ļū¶¾£¬øßĢśĖįÄĘ“¦Ąķ¹żµÄĖ®ÖŠŗ¬ÓŠĒāŃõ»ÆĢś½ŗĢ壬ÓĆ¼¤¹ā±ŹÕÕÉ䣬æÉŅŌ“Ó²ąĆę擵½Ņ»Ģõ¹āĀ·£¬ÕāøöĻÖĻóŌŚ»ÆѧÉĻ±»³ÉĪŖ___”£
£Ø3£©ĘÆ°×ŅŗŹĒŅ»ÖÖ³£ÓĆĻū¶¾¼Į£¬ĘäÖŠµÄÓŠŠ§³É·ÖŹĒ___£ØŠ“³ö»ÆѧŹ½£©”£
£Ø4£©ĘÆ°×·ŪŅ²ŹĒ³£¼ūĻū¶¾¼Į”£¹¤ŅµÉĻŹ¹ÓĆĘÆ°×·ŪŅ»°ć¼ÓČėÉŁĮæŃĪĖį»ņ“×Ėį£¬“ŁŹ¹___£ØĢīŠ“³öĪļÖŹĆū³Ę£©²śÉś£¬ŅŌŌöĒæĘÆ°×ɱ¾ś×÷ÓĆ”£ĒėÓĆ»Æѧ·½³ĢŹ½±ķŹ¾¼ŅÓĆĘÆ°×·Ū²»¼ÓČėĖįČēŗĪ²śÉśøĆĪļÖŹ___”£
£Ø5£©ĘÆ°×·ŪµÄÖŹĮæææĖüµÄ”°ÓŠŠ§ĀČ”±ŗāĮ攣ӊŠ§ĀČŹĒøł¾ŻĖüĶ¬ŃĪĖį×÷ÓĆŹ±²śÉśµÄĀČĘųĮæĄ“¼ĘĖćµÄ”£ĒėÅäĘ½Ķź³ÉøĆ¹ż³ĢµÄ»Æѧ·½³ĢŹ½£ŗ__Ca(ClO)2+__HCl=__Cl2”ü+__CaCl2+__”£Éś³ÉµÄĪ¢ĮæĀČĘųÓėĒāµāĖį·“Ó¦£¬æÉŅŌµĆµ½µāµ„ÖŹ£¬·“Ӧɜ³ÉµÄµāÓėNa2S2O3æÉŅŌ¶ØĮæµÄ½ųŠŠ·“Ó¦£ŗ2Na2S2O3+I2=Na2S4O6+2NaI£¬ĘÆ°×·ŪµÄÓŠŠ§ĀČ=£ØĘÆ°×·Ū¼ÓĖįĖłŹĶ·Å³öµÄĀČĘųµÄÖŹĮæ/ĘÆ°×·ŪµÄÖŹĮ棩”Į100%”£ĘÆ°×·ŪµÄÓŠŠ§ĀČŅ»°ćøßÓŚ30%£¬Ä³»Æ¹¤³§ĘÆ°×·Ū2g½ųŠŠÉĻŹöŅ»ĻµĮŠ·“Ó¦½ųŠŠ²ā¶Ø£¬ĻūŗÄĮņ“śĮņĖįÄĘ0.02mol£¬ŌņĘäÓŠŠ§ĀČĪŖ___”£
”¾“š°ø”æB”¢C”¢E ¶”“ļ¶ūŠ§Ó¦ NaClO HClO Ca(ClO)2+CO2+H2O=CaCO3”ż+2HClO 1 4 2 1 2H2O 35.5%
”¾½āĪö”æ
£Ø1£©×ŌĄ“Ė®Ļū¶¾¼Į¾ßÓŠŃõ»Æ×÷ÓĆ£¬ÄÜŹ¹Ī¢ÉśĪļŹ§Č„ÉśĄķ»īŠŌ£¬“Ó¶ųĘšµ½Ļū¶¾µÄ×÷ÓĆ”£
£Ø2£©ÓĆ¼¤¹ā±ŹÕÕÉ䣬æÉŅŌ“Ó²ąĆę擵½Ņ»Ģõ¹āĀ·£¬ÕāøöĻÖĻóĪŖ¶”“ļ¶ūŠ§Ó¦£»
£Ø3£©½«ĀČĘųĶØČėµ½ĒāŃõ»ÆÄĘČÜŅŗÖŠæÉÖĘ×÷ĘÆ°×Ņŗ£»
£Ø4£©½«ĀČĘųĶØČėŹÆ»ŅČéÖŠæÉÖĘČ”ĘÆ°×·Ū£¬ĘÆ°×·ŪµÄÓŠŠ§³É·ÖŹĒ“ĪĀČĖįøĘ£»
£Ø5£©øł¾Ż»ÆŗĻ¼ŪÉż½µŹŲŗćÅäĘ½øĆ·“Ó¦£»ĄūÓĆ·½³ĢŹ½Ķʵ¼³öø÷ĪļÖŹÖ®¼äµÄ¼ĘĮæ¹ŲĻµ£¬“śČėÓŠŠ§ĀČµÄ¼ĘĖć¹«Ź½ÖŠ½ųŠŠ¼ĘĖć”£
£Ø1£©Na2O2²»ÄÜÓĆÓŚ×ŌĄ“Ė®Ļū¶¾£¬ĘäÓėĖ®·“Ó¦»įÉś³ÉNaOH£¬¾ßÓŠøÆŹ“ŠŌ£¬²»ÄÜÓĆÓŚ×ŌĄ“Ė®µÄĻū¶¾£»Cl2O2¾ßÓŠĒæŃõ»ÆŠŌ£¬æÉÓĆÓŚ×ŌĄ“Ė®Ļū¶¾£»O3¾ßÓŠ½ĻĒæµÄŃõ»ÆŠŌ£¬ĒŅ·“Ó¦ŗó²śĪļĪŖO2£¬¶ŌČĖĢåĪŽÓ°Ļģ£¬æÉÓĆÓŚ×ŌĄ“Ė®µÄĻū¶¾£»O2Ńõ»ÆŠŌ½ĻČõ£¬ĪŽ·ØĻū¶¾É±¾ś£»ClO2¾ßÓŠ½ĻĒæµÄŃõ»ÆŠŌ£¬æÉÓĆÓŚ×ŌĄ“Ė®µÄĻū¶¾£»Ņņ“ĖæÉÓĆÓŚ×ŌĄ“Ė®Ļū¶¾µÄŹĒCl2O2”¢O3ŗĶClO2£¬ŹĒB”¢C”¢E£»
£Ø2£©ÓĆ¼¤¹ā±ŹÕÕÉ䣬æÉŅŌ“Ó²ąĆę擵½Ņ»Ģõ¹āĀ·£¬ÕāøöĻÖĻóŌŚ»ÆѧÉĻ±»³ÉĪŖ¶”“ļ¶ūŠ§Ó¦£»
£Ø3£©½«ĀČĘųĶØČėµ½ĒāŃõ»ÆÄĘČÜŅŗÖŠ£¬Éś³ÉĀČ»ÆÄĘŗĶ“ĪĀČĖįÄĘ£¬ŅŌ“ĪĀČĖįÄĘĪŖÖ÷ŅŖ³É·ÖµÄĪļÖŹĪŖĘÆ°×Ņŗ£»
£Ø4£©Ź¹ÓĆĘÆ°×·ŪŅ»°ć¼ÓČėÉŁĮæŃĪĖį»ņ“×Ėį£¬Óė“ĪĀČĖįøĘ·“Ӧɜ³É¾ßÓŠĒæŃõ»ÆŠŌµÄHClO£»¼ŅÓĆĘÆ°×·ŪÓėæÕĘųÖŠµÄCO2·“Ó¦æÉÉś³ÉHClO£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗCa(ClO)2+CO2+H2O=CaCO3”ż+2HclO”£
£Ø5£©“ĪĀČĖįøĘÓėŃĪĖį·“Ó¦£¬Éś³ÉĀČĘų”¢ĀČ»ÆøĘŗĶĖ®£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗCa(ClO)2+4HCl£½2Cl2”ü+CaCl2+2H2O£»øł¾Ż·½³ĢŹ½æɵĆ2Na2S2O3”«I2”«Cl2£¬ĻūŗÄĮņ“śĮņĖįÄĘ0.02molŹ±æÉÉś³ÉĀČĘų0.01mol, Éś³ÉĀČĘųµÄÖŹĮæĪŖ£ŗ0.01mol”Į71g/mol=0.71g£¬ÓŠŠ§ĀČ=![]() ”Į100%=35.5%”£
”Į100%=35.5%”£


 ѧ¶ųÓÅĻĪ½Ó½Ģ²ÄÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø
ѧ¶ųÓÅĻĪ½Ó½Ģ²ÄÄĻ¾©“óѧ³ö°ęÉēĻµĮŠ“š°ø Š”ѧæĪĢĆ×÷ŅµĻµĮŠ“š°ø
Š”ѧæĪĢĆ×÷ŅµĻµĮŠ“š°ø ½š²©ŹæŅ»µćČ«ĶØĻµĮŠ“š°ø
½š²©ŹæŅ»µćČ«ĶØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”涞Ńõ»ÆĮņµÄ“ß»ÆŃõ»ÆŹĒ¹¤ŅµÉĻÉś²śĮņĖįµÄÖ÷ŅŖ·“Ó¦£¬·“Ó¦ČēĻĀ£ŗ2SO2(g)+O2(g)![]() 2SO3(g) ”÷H1=£197.7kJ”¤mol£1 K1(ÅضČĘ½ŗā³£Źż)
2SO3(g) ”÷H1=£197.7kJ”¤mol£1 K1(ÅضČĘ½ŗā³£Źż)
ĪŖŃŠ¾æøĆ·“Ó¦£¬Ä³Ķ¬Ń§Éč¼ĘĮĖŅŌĻĀČżÖÖŅŃ×°¹ĢĢåV2O3“߻ƼĮµÄĆܱÕČŻĘ÷×°ÖĆ

(1)ŌŚ³õŹ¼Ģå»żÓėĪĀ¶ČĻąĶ¬µÄĢõ¼žĻĀ£¬¼×”¢ŅŅ”¢±ūÖŠ¾ł°“2 mol SO2”¢1molO2Ķ¶ĮĻ£¬“ļĘ½ŗāŹ±£¬ČżøöČŻĘ÷ÖŠSO2µÄ×Ŗ»ÆĀŹ“ӓ󵽊”µÄĖ³ŠņĪŖ___________________(ÓĆ”°¼×”¢ŅŅ”¢±ū”±±ķŹ¾)”£
(2)ŌŚČŻĘ÷±ūÖŠ£¬0.1MPaĢõ¼žĻĀ£¬ŌŚ²»Ķ¬ĪĀ¶Č»ņ²»Ķ¬Ķ¶ĮĻ·½Ź½ĻĀŃŠ¾æÉĻŹö·“Ó¦µĆµ½Źż¾ŻČēĻĀ±ķ£ŗ
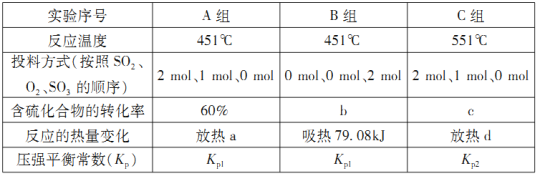
¢Ł±ķÖŠ£ŗa=___________£»b=___________”£
¢ŚŅŃÖŖÓĆĘ½ŗā·ÖŃ¹(·ÖŃ¹=×ÜŃ¹”ĮĪļÖŹµÄĮæ·ÖŹż)“śĢęĘ½ŗāÅØ¶Č¼ĘĖć£¬µĆµ½µÄĘ½ŗā³£Źż¼“ĪŖŃ¹ĒæĘ½ŗā³£Źż£¬ŌņKp1___________Kp2(Ģī”°>”±”¢”°<”±»ņ”°=”±)”£
¢Ū451”ę£¬Čō°“0.4 mol SO2”¢0.4molO2”¢0.4 mol SO3½ųŠŠĶ¶ĮĻ£¬Ōņ·“Ó¦æŖŹ¼Ź±vÕż(SO2)_______vÄę(SO2)(Ģī”°>”±”¢”°<”±»ņ”°=”±)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀČĖį¼ŲŹĒ³£¼ūµÄŃõ»Æ¼Į£¬ÓĆÓŚÖĘŌģ»šŅ©”¢ŃĢ»š”£¹¤ŅµÉĻÓĆŹÆ»ŅČéĀČ»Æ·ØÖʱøĀČĖį¼ŲµÄĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ
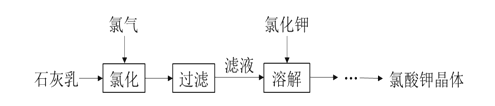
ŅŃÖŖ£ŗĀČ»Æ¹ż³ĢÖ÷ŅŖ·¢Éś·“Ó¦£ŗ![]()
Ķź³ÉĻĀĮŠĢīæÕ£ŗ
(1)¹¤ŅµÉś²śĀČĘųµÄ·½·ØŹĒ________£ØĒėÓĆĪÄ×Ö±ķŹö£©”£
(2)ĀČ»Æ¹ż³ĢŠčŅŖæŲÖĘ½ĻøßĪĀ¶Č£¬ĘäÄæµÄÓŠ£ŗ¢Ł_______£»¢Ś¼õÉŁCl2ÓėCa(OH)2Ö®¼äµÄø±·“Ó¦”£
(3)ĻņČȵÄĀĖŅŗÖŠ¼ÓČėÉŌ¹żĮæµÄĀČ»Æ¼Ų£¬“żČܽāĶźČ«ŗó½ųŠŠĄäČ“£¬ÓŠ“óĮæĀČĖį¼Ų¾§ĢåĪö³ö£¬Š“³öĻą¹Ų·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ______”£µĆµ½µÄĀČĖį¼Ų¾§ĢåÖŠæÉÄÜ»įŗ¬ÓŠÉŁĮæĀČ»Æ¼Ų£¬½ųŅ»²½Ģį“æµÄ·½·ØŹĒ_______”£
(4)ĪŖ²ā¶ØĖłµĆ¾§ĢåÖŠĀČĖį¼ŲµÄ“æ¶Č£¬½«a gѳʷÓėb g¶žŃõ»ÆĆĢ»ģŗĻ£¬¼ÓČČøĆ»ģŗĻĪļŅ»¶ĪŹ±¼äŗó£ØŌÓÖŹ²»²Ī¼Ó·“Ó¦£©ĄäČ“£¬³ĘĮæŹ£Óą¹ĢĢåÖŹĮ棬ÖŲø“¼ÓČČ”¢ĄäČ“”¢³ĘĮæ²Ł×÷£¬¼ĒĀ¼Źż¾ŻČēĻĀ±ķ£ŗ
¼ÓČČ“ĪŹż | µŚŅ»“Ī | µŚ¶ž“Ī | µŚČż“Ī | µŚĖÄ“Ī |
Ź£Óą¹ĢĢåÖŹĮæ£Øg£© | c | d | e | e |
(i)½ųŠŠ¼ÓČČ²Ł×÷Ź±£¬Ó¦½«¹ĢĢåÖĆÓŚ________£ØĢīŅĒĘ÷Ćū³Ę£©ÖŠ”£
(ii)øĆŹµŃé²»±Ų½ųŠŠµŚĪå“Ī¼ÓČȵÄŌŅņŹĒ_______”£
(iii)Čōij“Ī²ā¶Ø½į¹ūµÄĻą¶ŌĪó²īĪŖ-2.98%£¬Š“³öµ¼ÖĀÕāŅ»½į¹ūµÄŅ»ÖÖæÉÄÜĒéæö”£______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æLiAlH4ŹĒ½šŹō“¢Ēā²ÄĮĻ£¬ÓöĖ®ÄܾēĮŅ·“Ó¦ŹĶ·Å³öH2£¬LiAlH4ŌŚ125”ꏱ·Ö½āĪŖLiH”¢H2ŗĶAl”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.LiAlH4ŹŹŗĻÓĆ×÷Ńõ»Æ¼Į
B.1molLiAlH4Óė×ćĮæĖ®·“Ó¦×ŖŅĘ4øöµē×Ó
C.LiAlH4ŌŚ125”ꏱĶźČ«·Ö½ā£¬ĆæÉś³ÉŅ»øöH2·Ö×Ó×ŖŅĘ4molµē×Ó
D.ÓÉŅŌÉĻŠÅĻ¢æÉÖŖ£¬LiAlH4µÄ»¹ŌŠŌŠŌ±ČAlĒæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNaBH4Č¼ĮĻµē³Ų¾ßÓŠĄķĀŪµēŃ¹øß”¢ÄÜĮæĆܶȓóµČÓÅµć”£ŅŌøĆČ¼ĮĻµē³ŲĪŖµēŌ“µē½ā¾«Į¶ĶµÄ×°ÖĆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
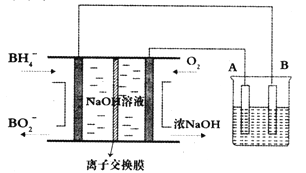
A. Ąė×Ó½»»»Ä¤Ó¦ĪŖŃōĄė×Ó½»»»Ä¤,Na+ÓÉ×ó¼«ŹŅĻņÓŅ¼«ŹŅĒØŅĘ
B. øĆČ¼ĮĻµē³ŲµÄøŗ¼«·“Ó¦Ź½ĪŖBH4-+8OH--8e-=BO2-+6H2O
C. µē½ā³ŲÖŠµÄµē½āÖŹČÜŅŗæÉŅŌŃ”ŌńCuSO4ČÜŅŗ
D. ĆæĻūŗÄ2.24LO2(±ź×¼×“æö)Ź±£¬Aµē¼«µÄÖŹĮæ¼õĒį12.8g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĻĀĮŠ·“Ó¦ÖŠ£¬HCl×÷Ńõ»Æ¼ĮµÄŹĒ£Ø””””£©
A.NaOH+HCl=NaCl+H2O
B.Zn+2HCl=ZnCl2+H2ӟ
C.MnO2+4HCl£ØÅØ£©![]() MnCl2+2H2O+Cl2”ü
MnCl2+2H2O+Cl2ӟ
D.CuO+2HCl=CuCl2+H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æļČ(Sr)ĪŖµŚ5ÖÜĘŚ¢ņA×åŌŖĖŲ”£øß“æĮłĖ®ĀČ»ÆļČ¾§Ģå(SrCl2”¤6H2O)¾ßÓŠŗÜøߵľ¼Ć¼ŪÖµ£¬61”ꏱ¾§ĢåæŖŹ¼Ź§Č„½į¾§Ė®£¬100”ꏱŹ§Č„Č«²æ½į¾§Ė®”£ÓĆ¹¤ŅµĢ¼ĖįļČ·ŪÄ©£Øŗ¬ÉŁĮæBa”¢FeµÄ»ÆŗĻĪļµČŌÓÖŹ£©Öʱøøß“æĮłĖ®ĀČ»ÆļČ¾§ĢåµÄ¹ż³ĢČēĻĀĶ¼ĖłŹ¾”£
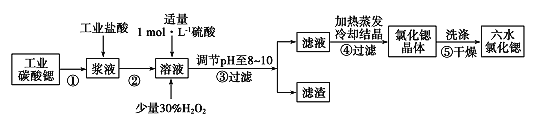
Ēė»Ų“š£ŗ
£Ø1£©³£ĪĀĻĀ£¬ĀČ»ÆļČČÜŅŗpH____7£ØŅŃÖŖ½šŹōŠŌCa<Sr£©£ØĢī”°“óÓŚ”±”¢”°µČÓŚ”±»ņ”°Š”ÓŚ”±£©£»
£Ø2£©Š“³öŌŚ½¬ŅŗÖŠ¼ÓČėŃĪĖįŹ±Ö÷ŅŖ·¢ÉśµÄĄė×Ó·½³ĢŹ½________£»
£Ø3£©²½Öč¢ŪĖłµĆĀĖŌüµÄÖ÷ŅŖ³É·ÖŹĒ______£ØĢī»ÆѧŹ½£©£¬µ÷½ŚČÜŅŗpHÖĮ8”«10£¬ŅĖŃ”ÓƵďŌ¼ĮĪŖ ______”£
A.Ļ”ĮņĖį B£®ĒāŃõ»ÆļČ·ŪÄ© C£®ĒāŃõ»ÆÄĘ D£®Ńõ»ÆļČ·ŪÄ©
£Ø4£©²½Öč¢ŻÖŠ£¬Ļ“µÓĀČ»ÆļČ¾§Ģå×īŗĆŃ”ÓĆ____”£
A£®Ė® B£®Ļ”ĮņĖį C£®ĒāŃõ»ÆÄĘČÜŅŗ D£®ĀČ»Æļȱ„ŗĶČÜŅŗ
£Ø5£©¹¤ŅµÉĻÓĆČČ·ē“µøÉĮłĖ®ĀČ»ÆļČ£¬Ń”ŌńµÄŹŹŅĖĪĀ¶Č·¶Ī§ŹĒ____£ØĢī×ÖÄø£©”£
A£®50”«60”ę B£®70”«80”ę C£®80”«100”ę D£®100”ęŅŌÉĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ(””””)
A.1 mol NaClÖŠŗ¬ÓŠNaCl·Ö×ÓŹżĪŖNA
B.ŹŅĪĀĻĀ£¬1 L pH=13µÄNaOHČÜŅŗÖŠ£¬ÓÉĖ®µēĄėµÄOH-ŹżÄæĪŖ0.1NA
C.1 mol FeøßĪĀĢõ¼žĻĀÓėĖ®ÕōĘų·“Ó¦£¬µē×Ó×ŖŅĘŹżĪŖ3NA
D.12 gŹÆÄ«Ļ©(µ„²ćŹÆÄ«)ÖŠŗ¬ÓŠĮłŌŖ»·µÄøöŹżĪŖ0.5NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹śæĘѧ¼ŅŃŠÖĘ³öŅ»Ö֓߻ƼĮ£¬ÄÜŌŚŹŅĪĀĻĀøߊ§“ß»ÆæÕĘųÖŠ¼×Č©µÄŃõ»Æ£¬Ęä·“Ó¦ČēĻĀ£ŗHCHO£«O2![]() CO2£«H2O ”÷H<0”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ( )
CO2£«H2O ”÷H<0”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ( )
A. øĆ·“Ó¦ĪŖĪüČČ·“Ó¦
B. CO2·Ö×ÓÖŠµÄ»Æѧ¼üĪŖ·Ē¼«ŠŌ¼ü
C. HCHO·Ö×ÓÖŠ¼Čŗ¬¦Ņ¼üÓÖŗ¬¦Š¼ü
D. ĆæÉś³É1.8g H2OĻūŗÄ2.24 L O2
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com