
在同温同压下,A容器中的氧气(O2)和B容器中的氨气(NH3)所含的原子个数相同,则A、B两容器中气体的体积之比是( )
|
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
科目:高中化学 来源: 题型:
下列电离方程式正确的是( )
A.MgSO4 = Mg2+ + SO42- B.Ba(OH)2 = Ba2+ + OH2-
C.Al2(SO4)3 = 2 Al+3 + 3 SO42- D.KClO3 = K+ + Cl- + 3 O2-
查看答案和解析>>
科目:高中化学 来源: 题型:
在Al2(SO4)3和MgSO4组成的混合物中,Al3 +与Mg2+的物质的量之比为2
+与Mg2+的物质的量之比为2 ∶3,则在含有2 mol SO
∶3,则在含有2 mol SO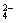 的混合物中,MgSO4的质量是多少克?
的混合物中,MgSO4的质量是多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中均需要的仪器是( )
①配制一定物质的量浓度的溶液 ②PH试纸的使用 ③过滤 ④蒸发.
|
| A. | 试管 | B. | 胶头滴管 | C. | 玻璃棒 | D. | 漏斗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 氢氧化钠的摩尔质量是40g |
|
| B. | 1molNaOH的质量是40g/mol |
|
| C. | 1gH2和1gN2所含分子数相等 |
|
| D. | 阿伏伽德罗常数个钠原子的质量是23g |
查看答案和解析>>
科目:高中化学 来源: 题型:
混合气体由O2和CH4组成,测得混合气体在标准状况下的密度为1.25g/L,则混合气体中O2和CH4的体积之比为( )
|
| A. | 3:1 | B. | 1:3 | C. | 4:1 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的 pH 在 5.0~6.0 之间,通过电解生成 Fe(OH)3 沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成 浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置如图所示: (1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,则无法使悬浮物形成浮渣。
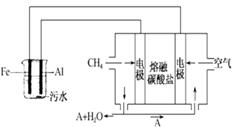

此时,应向污水中加入适量的_________。
a. H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
(2)电解池阳极的电极反应分别是①______________;
②4OH--4e-=2H2O+O2↑
(3)电极反应①和②的生成物反应得到 Fe(OH)3 沉淀的离子方程式是__________。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质,以 CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是 CH4+4CO2-8e-===5CO2+2H2O。
①正极的电极反应是______________。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。 则 A 物质的化学式是___________。
(5)实验过程中,若在阴极产生了 44.8L(标准状况)气体,则熔融盐燃料电池消耗 CH4_____L(标准状况)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com