
 .
. CH3COOC2H5+H2O,该反应类型是酯化(取代)反应.
CH3COOC2H5+H2O,该反应类型是酯化(取代)反应. 2CH3CHO+2H2O.
2CH3CHO+2H2O.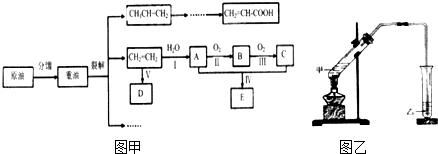
分析 乙烯含有碳碳双键,能发生加聚反应,生成聚乙烯,则D是聚乙烯.乙烯和水发生加成反应生成乙醇,则A是乙醇.乙醇发生氧化反应生成B,所以B是乙醛.乙醛继续被氧化生成乙酸,所以C是乙酸.乙酸和乙醇发生酯化反应生成乙酸乙酯,则E是乙酸,以此解答(1)(3);
(2)中制备乙酸乙酯由于生成的乙酸乙酯中含有乙酸和乙醇,二者都是与水互溶的,吸收装置中如果直接插入到碳酸钠溶液中,容易引起倒吸.
解答 解:石油分馏时不产生新物质,重油裂解生成的乙烯和水发生加成反应生成A乙醇,铜或银作催化剂、加热条件下,乙醇被氧气氧化生成乙醛和水,反应方程式为:
2CH3CH2OH+O2$→_{△}^{Cu/或Ag}$2CH3CHO+2H2O,B为CH3CHO,B催化氧化生成C,C为乙酸,在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯和水,E为乙酸乙酯,反应方程式为:CH3COOH+C2H5OH CH3COOC2H5+H2O,
CH3COOC2H5+H2O,
(1)乙烯发生加聚反应的化学方程式为 ,聚乙烯结构简式为:
,聚乙烯结构简式为: ,
,
故答案为: ;
;
(2)①C和A反应生成C是乙酸与乙醇反应生成乙酸乙酯,反应方程式为 CH3COOH+C2H5OH CH3COOC2H5+H2O,该反应的类型为酯化(取代)反应,
CH3COOC2H5+H2O,该反应的类型为酯化(取代)反应,
故答案为:CH3COOH+C2H5OH CH3COOC2H5+H2O;酯化(取代)反应;
CH3COOC2H5+H2O;酯化(取代)反应;
②由于乙醇和乙酸易溶于饱和碳酸钠溶液,若导管末端若插入液面以下,容易发生倒吸现象,所以导管不能插入液面以下,
故答案为:乙试管中导管插入液面下;
③乙为饱和碳酸钠溶液,可溶解乙醇,中和乙酸,易乙酸乙酯不溶于饱和碳酸钠溶液,可用分液的方法分离,
故答案为:溶解乙醇,中和乙酸,降低乙酸乙酯的溶解性;分液;
(3)反应Ⅰ为乙烯与水的加成反应,方程式为CH2=CH2+H2O $\stackrel{一定条件}{→}$CH2CH3OH,反应Ⅱ为乙醇的催化氧化,生成乙醛,方程式为2CH3CH2OH+O2 2CH3CHO+2H2O,
2CH3CHO+2H2O,
故答案为:CH2=CH2+H2O $\stackrel{一定条件}{→}$CH2CH3OH;2CH3CH2OH+O2 2CH3CHO+2H2O.
2CH3CHO+2H2O.
点评 本题考查有机推断,涉及烯烃、醇、醛、羧酸等性质,是对有机化合物知识的综合考查,能较好的考查考生的思维能力,题目难度不大,属于高考热点基础题型.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 945 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 升高温度可加快逆反应速率但不能改变正反应速率 | |
| C. | 一定条件下,SO2可100%转化为SO3 | |
| D. | 任何条件下,反应达到平衡,SO2的浓度一定等于SO3的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
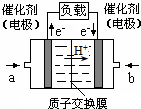 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子.电子经外电路、质子经内电路到达另一极与氧气反应.该电池总反应式为:2CH3OH+3O2═2CO2+4H2O.下列说法中正确的是( )| A. | 右边的电极为电池的负极,b处通入的是空气 | |
| B. | 左边的电极为电池的负极,a处通入的是甲醇 | |
| C. | 电池负极的反应式为:CH3OH+H2O═CO2+6H++4e- | |
| D. | 电池正极的反应式为:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3CH3 | D. | CH3CH2CH=CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水的离子积常数KW随着温度的升高而增大,说明水的电离过程是吸热的 | |
| B. | 弱电解质溶液稀释后,溶液中各种离子浓度一定都减小 | |
| C. | 某盐的水溶液呈酸性,该盐一定是强酸弱碱盐 | |
| D. | 中和相同体积相同pH的盐酸和醋酸溶液所需NaOH的物质的量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+) | B. | $\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ | C. | $\frac{c(C{H}_{3}CO{O}^{-})}{c({H}^{+})}$ | D. | Ka(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
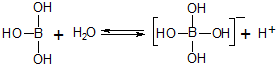
| A. | 硼酸加入水中抑制水的电离 | |
| B. | 硼酸是三元酸 | |
| C. | 硼酸与强碱在溶液中反应:H3BO3+OH-═[B(OH)4]- | |
| D. | 硼酸是两性化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com