
A、CO+CuO
| ||||
| B、2FeCl2+Cl2=2FeCl3 | ||||
| C、CaO+H2O=Ca(OH)2 | ||||
| D、2Al+3CuSO4=3Cu+2Al2(SO4)3 |
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 |
| B、0.2 mol?L-1 |
| C、0.4 mol?L-1 |
| D、0.8 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
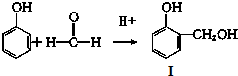
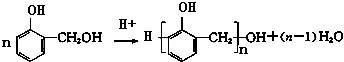
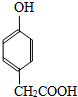 也能与CH3CHO发生类似反应①的反应,生成有机物Ⅲ,该反应化学方程式为
也能与CH3CHO发生类似反应①的反应,生成有机物Ⅲ,该反应化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸、氨水、硫酸钡均属于弱电解质、 |
| B、铜合金、铝合金、钢铁均属于金属材料 |
| C、动物油、植物油、矿物油均属于酯类化合物 |
| D、稀豆浆、稀盐酸、硅胶均属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2在反应中是还原剂 |
| B、每摩尔Na2O2完全反应时转移电子1mol |
| C、反应中O2既是氧化产物,又是还原产物 |
| D、上述反应可用于潜水艇中提供氧气 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,滴加足量蒸馏水,然后将所得溶液分别置于A、B试管中. | 固体物质全部完全溶解 |
| 步骤2:向A试管中滴加适量BaCl2溶液. | a.如果 b.如果 |
| 步骤3: | 有白色沉淀生成,C的成分有NaCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com