
| V |
| Vm |
| 8.96L |
| 22.4L/mol |
| 22.4L |
| 22.4L/mol |
|


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
| A、CS2分子的立体构型为V形 |
| B、ClO3-的空间构型为平面三角形 |
| C、CH4和SO32-的中心原子均为sp3杂化 |
| D、PCl5中所有原子均满足最外层8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①中的I2为固态,②中的I2为气态 |
| B、②的反应物总能量比①的反应物总能量低 |
| C、①的产物比②的产物热稳定性更好 |
| D、1 mol固态碘升华时将吸热17 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1:2 |
| B、1:1:1 |
| C、4:2:1 |
| D、1:2:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
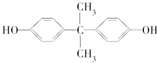 ).聚碳酸酯不耐高温,100℃时释放出的双酚A是25℃时的50倍.双酚A进入人体后,会溶解在身体的血管里,导致致命性的血管疾病.请回答下列问题:
).聚碳酸酯不耐高温,100℃时释放出的双酚A是25℃时的50倍.双酚A进入人体后,会溶解在身体的血管里,导致致命性的血管疾病.请回答下列问题: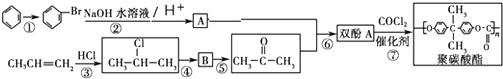
查看答案和解析>>
科目:高中化学 来源: 题型:
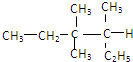 无标题的正确的名称是( )
无标题的正确的名称是( )| A、3,3-二甲基-4-乙基戊烷 |
| B、3,3-二甲基-2-乙基戊烷 |
| C、3,4,4-三甲基己烷 |
| D、3,3,4-三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
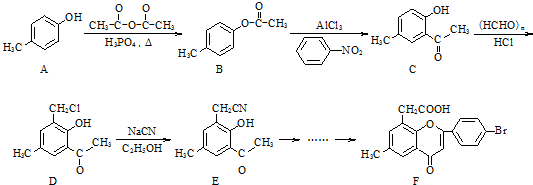
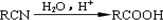
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 发生的现象 | 解释或结论 |
| A | 将溴乙烷与NaOH乙醇溶液加热产生的气体通入高锰酸钾溶液 | 高锰酸钾溶液颜色变浅 | 不能说明有乙烯产生 |
| B | 将一定量铁粉和铜粉的混合物加入由稀H2SO4和稀HNO3组成的混合溶液中 | 充分反应后,有金属粉末剩余 | 往反应后的溶液中加入足量的稀H2SO4,则金属粉末的质量一定不会减少 |
| C | 将一段用砂纸打磨过的镁条放入盛有热水的试管中 | 镁条表面立即有大量气泡和白色沉淀生成 | 镁和水反应生成了H2和Mg(OH)2 |
| D | 向某溶液中加入BaCl2溶液,再滴加稀硝酸 | 产生白色沉淀 | 则原溶液中含有SO42- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com