
 O2(g)=CO2(g);△H=-282.85kj.
O2(g)=CO2(g);△H=-282.85kj. O2(g)=H2O(l);△H=-285.8kj.该水煤气是由H2、N2、CO和CO2组成的混合气体.通入60LO2中燃烧后得到65L气体,再与NaOH溶液振荡后体积变为20L(以上体积均在标准状况下测定).这种水煤气中各种气体的体积是多少?
O2(g)=H2O(l);△H=-285.8kj.该水煤气是由H2、N2、CO和CO2组成的混合气体.通入60LO2中燃烧后得到65L气体,再与NaOH溶液振荡后体积变为20L(以上体积均在标准状况下测定).这种水煤气中各种气体的体积是多少? O2(g)=CO2(g);△H=-282.85kJ/mol
O2(g)=CO2(g);△H=-282.85kJ/mol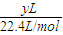 m
m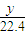 ×282.85kJ
×282.85kJ O2(g)=H2O(l);△H=-285.8kJ/mol
O2(g)=H2O(l);△H=-285.8kJ/mol n
n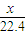 ×285.8kJ
×285.8kJ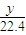 ×282.85kJ+
×282.85kJ+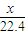 ×285.8kJ=1143.3…①
×285.8kJ=1143.3…① O2(g)=CO2(g) 体积减少△V
O2(g)=CO2(g) 体积减少△V O2(g)=H2O(l)体积减少△V
O2(g)=H2O(l)体积减少△V

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
100L水煤气燃烧后共放出热量1143.3kJ。
CO(g)+1/2 O2(g)=CO2(g);△H=-282.85kJ
H2(g)+1/2 O2(g)=H2O(l);△H=-285.8kJ
该水煤气是由H2、N2、CO和CO2组成的混合气体。通入60LO2中燃烧后得到65L气体,再与NaOH溶液振荡后体积变为20L(以上体积均在标准状况下测定)。这种水煤气中各种气体的体积是多少?
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com