
 共5mol,完全燃烧生成CO2和气态水时,则放出热量(
共5mol,完全燃烧生成CO2和气态水时,则放出热量( Q)的取值范围是 ;若生成CO2和H2O的物质的量相等,则放出的热量是 。
Q)的取值范围是 ;若生成CO2和H2O的物质的量相等,则放出的热量是 。科目:高中化学 来源:不详 题型:单选题
| A.在相同的条件下,2mol 氢气与 1 mol 氧气的总能量小于2mol 水蒸气的总能量 |
| B.H2(g)+1/2 O2(g)→H2O(1)+Q1;Q1>241.8kJ |
| C.H2(g)+ 1/2O2(g)→H2O(1)+Q2;Q2<241.8kJ |
| D.任何条件下,2L水蒸气分解成2L氢气与1L氧气需吸收483.6kJ热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
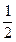 O2(g)====H2O(l)△H=-285kJ·mol-1
O2(g)====H2O(l)△H=-285kJ·mol-1 )+5O2(g)====3CO2(g)+4H2O(l)△H=-2220.0kJ·mol-1
)+5O2(g)====3CO2(g)+4H2O(l)△H=-2220.0kJ·mol-1 )====H2O(g) △H=+44.0kJ·mol-1,写出丙烷燃烧生成CO2和气态水的热化学方程式_________________________________________。
)====H2O(g) △H=+44.0kJ·mol-1,写出丙烷燃烧生成CO2和气态水的热化学方程式_________________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
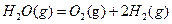 △H1
△H1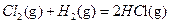 △H2
△H2 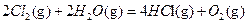 △H3
△H3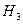 与⊿
与⊿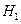 和⊿
和⊿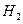 间的关系正确的是
间的关系正确的是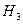 =⊿
=⊿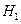 +2⊿
+2⊿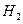 B ⊿
B ⊿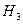 =⊿
=⊿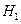 +⊿
+⊿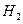
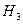 =⊿
=⊿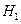 -2⊿
-2⊿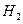 D. ⊿
D. ⊿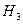 =⊿
=⊿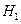 - ⊿
- ⊿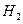
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
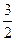 C(s)=
C(s)=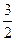 CO2(g)+2Fe(s) △H= +234.1kJ·mol-1 C(s) + O2(g) = CO2(g) △H=-39
CO2(g)+2Fe(s) △H= +234.1kJ·mol-1 C(s) + O2(g) = CO2(g) △H=-39 3.5kJ·mol-1 则2Fe(s)+
3.5kJ·mol-1 则2Fe(s)+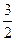 O2(g)= Fe2O3(s)的△H是
O2(g)= Fe2O3(s)的△H是
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g)
密闭容器中,充入1 mol CO2和3 mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol
CH3OH(g)+H2O(g) ΔH=-49.0kJ/mol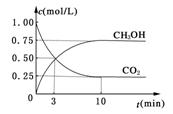
 n)。
n)。 ΔH=-1277 kJ·mol-1
ΔH=-1277 kJ·mol-1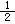 O2(g)=CO(g) ΔH=-110.5 kJ·mol-1
O2(g)=CO(g) ΔH=-110.5 kJ·mol-1 ,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。
,中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆。甲醇燃料电池的工作原理如下图所示。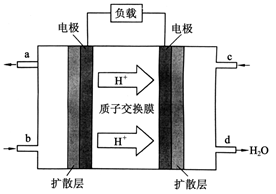

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com