
| A. | 锌是负极,发生氧化反应 | |
| B. | 锌的质量减少6.5g,外电路中通过0.4mol电子 | |
| C. | 溶液中OH-向正极移动,K+、H+向负极移动 | |
| D. | 随着电极反应的不断进行,电解质溶液中n(OH-)减小 |
分析 根据化合价变化可知Zn被氧化,应为原电池的负极,则正极为Ag2O,溶液中阴离子向负极移动,阳离子向正极移动.
解答 解:A、根据化合价变化可知Zn被氧化,应为原电池的负极,负极上失电子发生氧化反应,故A正确;
B、锌的质量减少6.5g,外电路中通过$\frac{6.5g}{65g/mol}$×2=0.2mol电子,故B错误;
C、溶液中阴离子向负极移动,阳离子向正极移动,故B错误;
D、随着反应的不断进行,负极上锌失电子和氢氧根离子反应生成氢氧化锌,所以导致溶液中氢氧根离子浓度降低,所以溶液的PH值减小,故D正确;
故选AD.
点评 本题考查了放热反应和原电池原理,为高考高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,明确原电池的构成、电极上发生的反应、电流的流向即可解答,难度不大.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:填空题
| 类别 | 编号 |
| 新能源 | |
| 常规能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成a mol A的同时消耗2a mol C | |
| B. | 混合气体的压强不再变化 | |
| C. | 单位时间内消耗a mol A的同时消耗a mol B | |
| D. | B气体的浓度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/浓度 | c(NH3)(mol/L) | c(O2 )(mol/L) | c(NO)(mol/L) |
| 起始 | 0.800 | 1.000 | 0.000 |
| 第2min | a | b | c |
| 第4min | 0.400 | 0.500 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 洗净的容量瓶中残留少量的蒸馏水 | B. | 溶解NaOH的烧杯未洗净 | ||
| C. | 称量NaOH时使用称量纸 | D. | 定容时俯视刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| Fe | Cu | Zn | Ag | Au | W | |
| 熔点/℃ | 1535 | 1083 | 419.5 | 960.8 | 1063 | 3380 |
| 沸点/℃ | 3000 | 2595 | 907 | 2212 | 2707 | 5627 |
| A. | Fe、Ag | B. | Ag、Au | C. | Zn、W | D. | Fe、Au |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
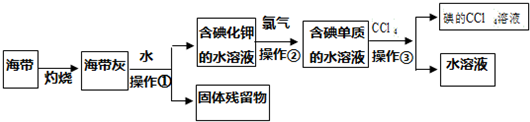
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com