
| A. | ①④⑤⑥ | B. | ②③⑥ | C. | ②④⑤⑥ | D. | 只有④ |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:①A为固态,反应正向进行时气体质量增大,逆向进行时气体质量减小,所以,密度不变时平衡,故①正确;
②该反应前后气体体积不变,所以压强不变是不一定平衡,故②错误;
③该反应前后气体物质的量相等,所以气体物质的量不变不一定平衡,故③错误;
④B的浓度不变,说明反应平衡了,故④正确;
⑤混合气体的平均相对分子质量不再改变的状态,说明气体的质量不变,正逆反应速率相等,反应达到平衡,故⑤正确;
⑥V正(B)=2V逆(C)时,说明正逆反应速率相等,反应平衡,故⑥正确.
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌.如图是过氧化氢法生产亚氯酸钠的工艺流程图:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌.如图是过氧化氢法生产亚氯酸钠的工艺流程图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. Al(OH)3+3H+(用离子方程式表示).
Al(OH)3+3H+(用离子方程式表示).| X | ||||
| Y | Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 二甲苯一溴代物的熔点/℃ | 234 | 206 | 213 | 204 | 214 | 205 |
| 对应的二甲苯的熔点/℃ | 13 | -54 | -27 | -54 | -27 | -54 |
| A. | 熔点为234℃的是一溴代间二甲苯 | B. | 熔点为234℃的是一溴代邻二甲苯 | ||
| C. | 熔点为-54℃的是间二甲苯 | D. | 熔点为-27℃的是对二甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 热稳定性:HF>HCl>HBr>HI | B. | 微粒半径:K+>Na+>Mg2+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4 | D. | 还原性:Al>Mg>Na |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;Na2O2的电子式:
;Na2O2的电子式: ,H2S的电子式:
,H2S的电子式:
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
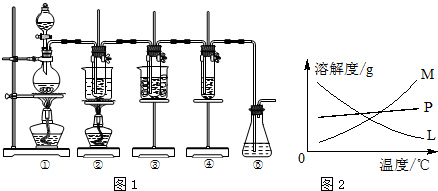
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
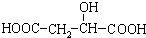 )广泛存在于水果中,尤以苹果、葡萄、西瓜、山
)广泛存在于水果中,尤以苹果、葡萄、西瓜、山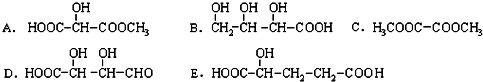
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com