

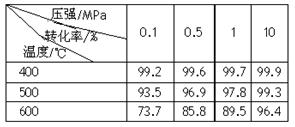
| A��400��500�� 0.1 MPa | B��400��10 MPa |
| C��500��10 MPa | D��400��500��1 MPa |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������Ƽ���ŵ��Ǽ����˶��豸�ĸ�ʴ |
| B����ҵ��������ʱ����98%��������������������Ա����γ���������������� |
| C���ϳɰ�����Ȼ�̵��ķ���֮һ |
| D��̼�����׳�С�մ�,������һ�������Դ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 4NO(g) +6H2O(l) ��H��0
4NO(g) +6H2O(l) ��H��0 2NO2(g) ��H��0
2NO2(g) ��H��0 2HNO3(l) +NO(g) ��H��0
2HNO3(l) +NO(g) ��H��0| A���ʵ������¶� |
| B���ʵ������������ڵ�ѹǿ |
| C�����������O2��Ũ�� |
| D�������������ɻ���������Һ�Ӵ��� |
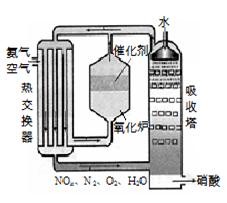
 m3�������蹤ҵ������������У�ͨ��ѭ����������ʹNH3��O2������ȫ���á�
m3�������蹤ҵ������������У�ͨ��ѭ����������ʹNH3��O2������ȫ���á��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
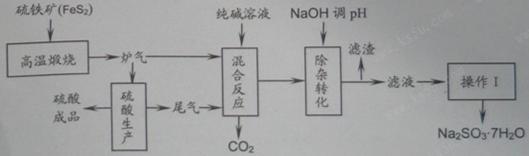
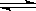 2SO3(g)���о����֣�SO3���������(SO3%)���¶�(T)�ı仯�����ߢ���ʾ�������ж���ȷ����________
2SO3(g)���о����֣�SO3���������(SO3%)���¶�(T)�ı仯�����ߢ���ʾ�������ж���ȷ����________
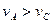
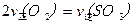
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CO2(g) + H2(g)����Ӧ�����������仯����ͼ��ʾ����500 ��ʱ��ƽ�ⳣ�� K = 9������2 L���ܱ�������CO��ˮ��������ʼŨ�ȶ���0.1 mol/L��10 minʱ�ﵽƽ��״̬��
CO2(g) + H2(g)����Ӧ�����������仯����ͼ��ʾ����500 ��ʱ��ƽ�ⳣ�� K = 9������2 L���ܱ�������CO��ˮ��������ʼŨ�ȶ���0.1 mol/L��10 minʱ�ﵽƽ��״̬��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
 Na2CO3���ڹ�ҵ����������������ҪӦ�ã���ʵ�����Ʒ���ҵ�Ʒ����£�
Na2CO3���ڹ�ҵ����������������ҪӦ�ã���ʵ�����Ʒ���ҵ�Ʒ����£� Na2CO3����
Na2CO3����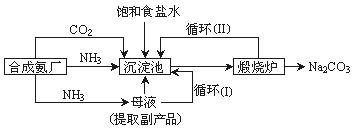
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
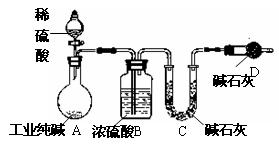
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��SO2��ʳƷ��ҵ�п���������������������Ư�ס� |
| B���ϳɰ���ҵ��Ҫ���¸�ѹ���� |
| C�����Ṥҵ����ˮ����SO3 |
| D�����Ṥҵ�з���¯�ų��Ŀ����ɹ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���ڢ� | B���٢� | C���٢� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com