
| A. | Na2S | B. | CuSO4 | C. | NaCl | D. | Na2SO4 |
分析 A、电解Na2S溶液时,阴极上析出氢气,阳极上得到硫单质,所以溶液中的氢氧根离子浓度增大;
B、电解CuSO4溶液时,阴极上析出铜,阳极上氢氧根离子失电子放出氧气,所以溶液中的氢离子浓度增大;
C、电解NaCl溶液时,阴极上析出氢气,阳极上得到氯气,所以溶液中的氢氧根离子浓度增大;
D、电解Na2SO4溶液时,实际上电解的是水,所以溶液中氢离子浓度不变.
解答 解:A、电解Na2S溶液时,阴极上析出氢气,阳极上得到硫单质,所以溶液中的氢氧根离子浓度增大,溶液的pH值增大,溶液的b>a,故A不符合;
B、电解CuSO4溶液时,阴极上析出铜,阳极上氢氧根离子失电子放出氧气,所以溶液中的氢离子浓度增大,溶液的pH值减小,溶液的b<a,故B符合;
C、电解NaCl溶液时,阴极上析出氢气,阳极上得到氯气,所以溶液中的氢氧根离子浓度增大,溶液的pH值增大,溶液的b>a,故C不符合;
D、电解Na2SO4溶液时,实际上电解的是水,所以溶液中氢离子浓度不变,故pH值不变,溶液的b=a,故D符合;
故选BD.
点评 本题考查了电解原理,随着电解的进行判断溶液pH值的变化,首先要知道离子的放电顺序、电解的实质,只有明白这些知识点才能正确解答,题目难度中等.


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:选择题
| A. | 此合金的熔点、硬度比镁和铝的熔点、硬度都高 | |
| B. | 此合金能全部溶解于稀盐酸中 | |
| C. | 此合金能全部溶解于氢氧化钠溶液中 | |
| D. | 比合金不能全部溶解于过量Fe2Cl3溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学键是一种作用力 | |
| B. | 氢键也属化学键 | |
| C. | 化学键可以使离子相结合,也可以使原子相结合 | |
| D. | 化学方应过程中,反应物分子内的化学键断裂,生成物中的化学键形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na2O2与H2O反应制备O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| B. | KHCO3溶液与Al2(SO4)3溶液混合:3HCO3-+Al3+=Al(OH)3↓+3CO2↑ | |
| C. | 将过量铁粉加入到稀硝酸中:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O | |
| D. | 碳酸电离:H2CO3=H++HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2使酸性KMnO4褪色:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ | |
| B. | Fe(OH)2与HNO3溶液的反应:Fe(OH)2+2H+=Fe2++2H2O | |
| C. | 足量NaOH与磷酸二氢铵反应:OH-+NH4+=NH3•H2O | |
| D. | 将SO2通入BaCl2溶液中:SO2+H2O+Ba2+=BaSO3↓+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(A-)<c(K+) | B. | c(H+)=c(OH-)<c(K+)<c(A-) | ||
| C. | V总≥20mL | D. | V总≤20mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硫酸和浓盐酸长期暴露在空气中浓度降低 | |
| B. | 氯水和活性炭使红墨水褪色 | |
| C. | 漂白粉和钠长期暴露在空气中变质 | |
| D. | 氯水和过氧化钠使品红褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
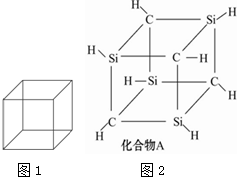
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com