
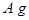 加入FeCl3和盐酸的混合液中,充分反应(不考虑水电离出的离子)。
加入FeCl3和盐酸的混合液中,充分反应(不考虑水电离出的离子)。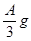 ,则溶液中的阳离子一定有 ,一定没有 ;
,则溶液中的阳离子一定有 ,一定没有 ;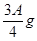 ,则溶液中的阳离子一定有_________,一定没有___________。
,则溶液中的阳离子一定有_________,一定没有___________。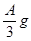 ,则剩余的固体一定是铜,则溶液中的阳离子一定有Zn2+、Fe2+;而一定没有铁离子,氢离子可能含有,也可能没有。
,则剩余的固体一定是铜,则溶液中的阳离子一定有Zn2+、Fe2+;而一定没有铁离子,氢离子可能含有,也可能没有。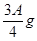 ,则剩余的固体中一定含有铜、铁和锌,所以溶液中的阳离子一定有Zn2+、Fe2+;而一定没有 Cu2+、H+、Fe3+。
,则剩余的固体中一定含有铜、铁和锌,所以溶液中的阳离子一定有Zn2+、Fe2+;而一定没有 Cu2+、H+、Fe3+。

科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.①④ | C.②③ | D.③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
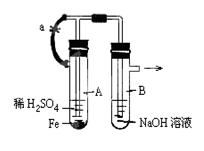
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
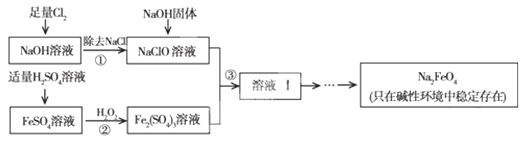
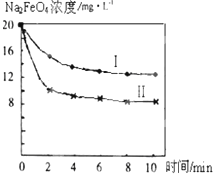
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.48 mol | B.0.42mol | C.0.32 mol | D.0.28 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com