
·ЦОц УГ»ҜС§КҪәНАлЧУ·ыәЕұнКҫөзАл№эіМөДКҪЧУЈ¬іЖОӘөзАл·ҪіМКҪЈ¬ұнКҫОпЦКИЬҪвУЪЛ®КұөзАліЙАлЧУөД»ҜС§·ҪіМКҪЈ»ЗвСх»ҜұөКЗЗҝјоНкИ«өзАлЈ¬БтЛбКЗЗҝЛбЈ¬НкИ«өзАлЈ¬БтЗв»ҜДЖЎўСЗБтЛбДЖКЗСОЈ¬КЗЗҝөзҪвЦКНкИ«өзАлЈ¬Т»Л®әП°ұЎўМјЛбКфУЪИхЛбҙжФЪөзАлЖҪәвЈ¬ҫЭҙЛҪшРР·ЦОцҪвҙрЈ®
Ҫвҙр ҪвЈәЈЁ1Ј©ЗвСх»ҜұөКЗЗҝөзҪвЦКЈ¬КЗУЙЗвСхёщАлЧУәНұөАлЧУ№№іЙЈ¬ДЬНкИ«өзАлЈ¬өзАл·ҪіМКҪОӘЈәBaЈЁOHЈ©2=Ba2++2OH-Ј¬
№Кҙр°ёОӘЈәBaЈЁOHЈ©2=Ba2++2OH-Ј»
ЈЁ2Ј©БтЛбКЗЗҝөзҪвЦКЈ¬ДЬНкИ«өзАлЈ¬өзАл·ҪіМКҪОӘЈәH2SO4=2H++SO42-Ј¬
№Кҙр°ёОӘЈәH2SO4=2H++SO42-Ј»
ЈЁ3Ј©NH3•H2OКЗИхөзҪвЦКІҝ·ЦөзАлЈ¬өзАл№эіМҝЙДжЈ¬өзАл·ҪіМКҪОӘЈәNH3•H2O?NH4++OH-Ј¬
№Кҙр°ёОӘЈәNH3•H2O?NH4++OH-Ј»
ЈЁ4Ј©H2CO3КЗИхЛбОӘИхөзҪвЦКЈ¬·ЦІҪөзАлЈ¬өзАл№эіМҝЙДжЈ¬өзАл·ҪіМКҪОӘЈәH2CO3?HCO3-+H+Ј¬HCO3-?H++CO32-Ј¬
№Кҙр°ёОӘЈәH2CO3?HCO3-+H+Ј¬HCO3-?H++CO32-Ј»
ЈЁ5Ј©NaHSКЗЗҝјоИхЛбСОЈ¬КфУЪЗҝөзҪвЦКНкИ«өзАлЈ¬HS-АлЧУІҝ·ЦөзАлЈ¬өзАл·ҪіМКҪОӘЈәNaHS=Na++HS-Ј¬HS-?H++S2-Ј¬
№Кҙр°ёОӘЈәNaHS=Na++HS-Ј»HS-?H++S2-Ј»
ЈЁ6Ј©NaHSO3КЗЗҝјоИхЛбСОЈ¬КфУЪЗҝөзҪвЦКНкИ«өзАлЈ¬HSO3-АлЧУІҝ·ЦөзАлЈ¬өзАл·ҪіМКҪОӘЈәNaHSO3=Na++HSO3-Ј¬HSO3-?H++SO32-Ј¬
№Кҙр°ёОӘЈәNaHSO3=Na++HSO3-Ј¬HSO3-?H++SO32-..
өгЖА ұҫМвҝјІйБЛөзАл·ҪіМКҪөДКйРҙЈ¬ХЖОХөзАл·ҪіМКҪөДКйРҙ·Ҫ·ЁІўДЬБй»оФЛУГКЗХэИ·ҪвҙрҙЛАаМвөД№ШјьЈ¬МвДҝДС¶ИІ»ҙуЈ®



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәСЎФсМв
| AЈ® | ҙУОпЦКөД·ЦАаҪЗ¶ИАҙҝҙЈ¬УНМхЕд·ҪЦРөДЎ°Гч·ҜЎўјоЎұҫщКфУЪСО | |
| BЈ® | ·ЕЦГ№эіМ·ўЙъөД·ҙУҰОӘСх»Ҝ»№Фӯ·ҙУҰ | |
| CЈ® | ·ЕЦГ№эіМ·ўЙъөД·ҙУҰЦР·ҙУҰОпәНЙъіЙОпҫщОӘөзҪвЦК | |
| DЈ® | ·ҙУҰөДАлЧУ·ҪіМКҪОӘЈә3CO32-+2KAlЈЁSO4Ј©2•12H2OЁT3Na2SO4+2K++4SO42-+3CO2Ўь+2AlЈЁOHЈ©3Ўэ+21 H2O |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә¶аСЎМв
| AЈ® | Cl2+2NaOHЁTNaCl+NaClO+H2O | BЈ® | Fe+CuSO4ЁTFeSO4+Cu | ||
| CЈ® | 2KClO3$\frac{\underline{MnO_2}}{Ўч}$2KCl+3O2Ўь | DЈ® | 3NO2+H2O=2HNO3+NO |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәМоҝХМв
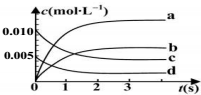 ФЪ2LГЬұХИЭЖчДЪЈ¬800ЎжКұ·ҙУҰЈә2N0ЈЁgЈ©+O2ЈЁgЈ©?2NO2ЈЁgЈ©МеПөЦРЈ¬nЈЁNOЈ©ЛжКұјдөДұд»ҜИзПВұнЈә
ФЪ2LГЬұХИЭЖчДЪЈ¬800ЎжКұ·ҙУҰЈә2N0ЈЁgЈ©+O2ЈЁgЈ©?2NO2ЈЁgЈ©МеПөЦРЈ¬nЈЁNOЈ©ЛжКұјдөДұд»ҜИзПВұнЈә| КұјдЈЁsЈ© | 0 | 1 | 2 | 3 | 4 | 5 |
| NЈЁNOЈ©ЈЁmolЈ© | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәКөСйМв
 ОӘБЛСРҫҝНвҪзМхјю¶Ф№эСх»ҜЗв·ЦҪвЛЩВКөДУ°ПмЈ¬ДіН¬С§ЧцБЛТФПВКөСйЈ¬Зл»ШҙрПВБРОКМвЈ®
ОӘБЛСРҫҝНвҪзМхјю¶Ф№эСх»ҜЗв·ЦҪвЛЩВКөДУ°ПмЈ¬ДіН¬С§ЧцБЛТФПВКөСйЈ¬Зл»ШҙрПВБРОКМвЈ®| ұаәЕ | ІЩЧч | КөСйПЦПу |
| ўЩ | ·ЦұрФЪКФ№ЬAЎўBЦРјУИл5mL 5% H2O2ИЬТәЈ¬ёчөОИл2өО1mol/L FeCl3ИЬТәЈ®ҙэКФ№ЬЦРҫщУРККБҝЖшЕЭіцПЦКұЈ¬Ҫ«КФ№ЬA·ЕИлКўУР5ЎжЧуУТАдЛ®өДЙХұӯЦРҪюЕЭЈ»Ҫ«КФ№ЬB·ЕИлКўУР40ЎжЧуУТИИЛ®өДЙХұӯЦРҪюЕЭЈ® | КФ№ЬAЦРІ»ФЩІъЙъЖшЕЭЈ» КФ№ЬBЦРІъЙъөДЖшЕЭБҝФцҙуЈ® |
| ўЪ | БнИЎБҪЦ§КФ№Ь·ЦұрјУИл5mL 5% H2O2ИЬТәәН5mL 10% H2O2ИЬТә | КФ№ЬAЎўBЦРҫщОҙГчПФјыөҪУРЖшЕЭІъЙъЈ® |

Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәСЎФсМв
| AЈ® |  ұнКҫұыП©өДјьПЯКҪ ұнКҫұыП©өДјьПЯКҪ | BЈ® |  ұнКҫјЧНй·ЦЧУЗт№чДЈРН ұнКҫјЧНй·ЦЧУЗт№чДЈРН | ||
| CЈ® | C2H4O2ұнКҫТТЛбөД·ЦЧУКҪ | DЈ® |  34S2-өДҪб№№КҫТвНј 34S2-өДҪб№№КҫТвНј |
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәҪвҙрМв
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәјЖЛгМв
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈәјЖЛгМв
Ійҝҙҙр°ёәНҪвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com