

| A. | 从KI和I2的固体混合物中回收I2,可使用如图甲所示实验装置 | |
| B. | 分离Na2CO3溶液和CH3COOC2H5,可使用如图乙所示实验装置 | |
| C. | 用图丙所示仪器配制0.150mol/LNaOH溶液 | |
| D. | 如图丁所示可用于实验室制氨气并收集干燥的氨气 |
分析 A.没有收集碘的装置;
B.Na2CO3溶液与CH3COOCH2CH3不互溶,可以使用分液方法分离;
C.精确配制应用容量瓶;
D.NH4Cl与Ca(OH)2 加热得到NH3,碱石灰干燥NH3,圆底烧瓶干燥收集NH3,水处理多余NH3.
解答 解:A.I2在加热过程中发生升华,但没有收集装置,故A错误;
B.Na2CO3溶液与CH3COOCH2CH3不互溶,可以使用分液方法分离,故B错误;
C.配制一定浓度的物质的量浓度的溶液应该用容量瓶而不是量筒,故C错误;
D.NH4Cl与Ca(OH)2 加热得到NH3,碱石灰干燥NH3,圆底烧瓶干燥收集NH3,水处理多余NH3,故D正确.
故选D.
点评 本题考查化学实验方案的评价,涉及物质的制备、分离、收集等,侧重于学生的分析能力和实验能力以及评价能力的考查,为高考高频考点和常见题型,注意把握实验的方案的合理性和实验操作的合理性,难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Y在空气中燃烧一定生成Y2O2 | B. | Z只能形成两种含氧酸根 | ||
| C. | X-半径一定比Y+半径大 | D. | W 的氢化物一定比Z的氢化物稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
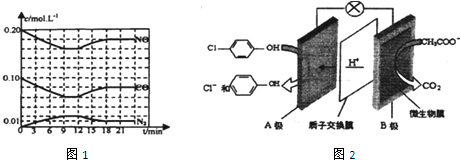
 )的酸性废水,可利用微生物电池法除去,其原理如图2所示
)的酸性废水,可利用微生物电池法除去,其原理如图2所示查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,将氨水与氯化铵溶液混合得到 c(NH3•H2O)+c(NH4+)=0.1mol•L-1的混合溶液.溶液中c(NH3•H2O)、c(NH4+)与pH的关系如图所示.下列有关离子浓度关系叙述一定正确的是( )
25℃时,将氨水与氯化铵溶液混合得到 c(NH3•H2O)+c(NH4+)=0.1mol•L-1的混合溶液.溶液中c(NH3•H2O)、c(NH4+)与pH的关系如图所示.下列有关离子浓度关系叙述一定正确的是( )| A. | W点表示溶液中:c(NH4+)+c(H+)=c(OH-) | |
| B. | pH=10.5溶液中:c(Cl-)+c(OH-)+c(NH3•H2O)<0.1 mol•L-1 | |
| C. | pH=9.5溶液中:c(NH3•H2O)>c(NH4+)>c(OH-)>c(H+) | |
| D. | 向W点所表示1L溶液中加入0.05molNaOH固体(忽略溶液体积变化):c(Cl-)>c(Na+)>c(OH-)>c(NH4+)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 地沟油经过处理,可用来制造肥皂 | |
| C. | 漂白粉长期暴露在空气中会变质失效 | |
| D. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 咖啡酸具有止血功效,存在于多种中药中,其结构简式如图:则下列有关说法正确的是( )
咖啡酸具有止血功效,存在于多种中药中,其结构简式如图:则下列有关说法正确的是( )| A. | 该物质中苯环上一氯化物有2种 | |
| B. | 所有碳原子不可能都在同一平面上 | |
| C. | 既能发生取代反应,也能发生加成反应 | |
| D. | 1mol该物质可以与1.5mol碳酸钠溶液反应生成1.5molCO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na+K+OH-Cl- | B. | Na+Cu2+SO42-NO3- | ||
| C. | K+ Na+ SO42- Cl- | D. | Ba2+ CO32- NO3- K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
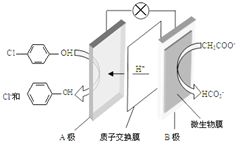 现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(
现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(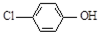 ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )| A. | 当外电路中有0.2mole-转移时,通过质子交换膜的H+的个数为0.2NA | |
| B. | A极的电极反应式为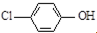 +e-═Cl-+ +e-═Cl-+ | |
| C. | 电流方向从B极沿导线经小灯泡流向A极 | |
| D. | B为电池的正极,发生还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com