


科目:高中化学 来源: 题型:
| A、纤维素属于多糖,在人体内水解转化为葡萄糖,也可为人类提供能量 |
| B、糖尿病患者吃糖量必须限制,但淀粉类食物不必进行限制 |
| C、同质量的脂肪在体内氧化放出的能量比糖类和蛋白质高得多,是提供能量的主要物质 |
| D、葡萄糖在人体内不可以转化为脂肪,所以吃糖不会使人发胖 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、142g |
| B、71g |
| C、0.05mol |
| D、0.025mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤ | B、②③ |
| C、①③④ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.012kg C-12(12C)所含有的碳原子物质的量为1mol |
| B、SO42-的摩尔质量是 98 g?mol-1 |
| C、1 mol任何气体所占体积都约是22.4 L |
| D、阿伏加德罗常数等于6.02×1023 mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
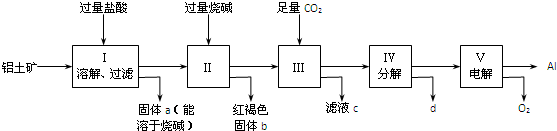
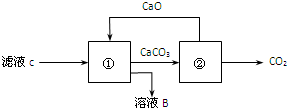
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在100℃、101 KPa条件下,1mol液态水汽化为水蒸气吸收的热量为40.69KJ,则H2O(g)?H2O(l) 的△H=-40.69KJ/mol |
| B、已知MgCO3的Ksp=6.82×10-4mol2/L2,则所有含固体MgCO3的溶液中,都有C(Mg 2+ )=C(CO32-),且 C(Mg2+)?C(CO32-)=6.82×10-4mol2/L2 |
| C、已知:C-C的键能348KJ/mol,C=C的键能610KJ/mol,C-H的键能413KJ/mol, H-H的键能436KJ/mol, 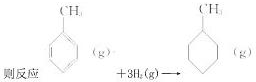 的焓变为:△H=[(4×348+3×610+8×413)+3×436-(7×348+14×413)]=-384 kJ/mol 的焓变为:△H=[(4×348+3×610+8×413)+3×436-(7×348+14×413)]=-384 kJ/mol |
| D、碳酸氢钠溶液中存在:c(H*)+c(H2CO3)=c(OH-)+c(CO32-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com