
 ��
��

 ��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
��ְٷְټ�����Ԫ��ĩ���Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
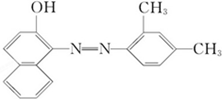
| A����������������� |
| B�����ڷ����� |
| C��1mol���л����к���18mol��̼ԭ�� |
| D�������������ڷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����NH5��Ԫ�ض��Ƿǽ��������ڹ��ۻ����� |
| B��NH5����Ԫ��Ϊ+1�� |
| C��NH5��ˮ�ķ�Ӧ��������ԭ��Ӧ |
| D��NH5����ˮ����Һ�ʼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
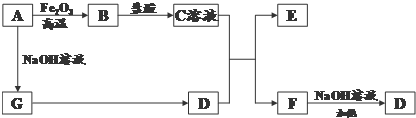
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1������Ҫ������������⣺
��1������Ҫ������������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ijѧϰС������ͼװ�òⶨ��þ�Ͻ������������������������ԭ��������
ijѧϰС������ͼװ�òⶨ��þ�Ͻ������������������������ԭ���������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
- 2 |
- 3 |
2- 3 |
| ʵ���� | HA���ʵ���Ũ�ȣ�mol/L�� | NaOH���ʵ���Ũ�ȣ�mol/L�� | �����Һ��pH |
| �� | 0.20 | 0.20 | pH=a |
| �� | 0.10 | 0.10 | pH=8.00 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������ԭ��Ӧ��ʵ���ǵ��ӵ�ת�� |
| B�������Ԫ�صĻ����������ǿ������ |
| C��ԭ��ʧ������Խ�࣬��Ԫ�صĽ����Ծ�Խǿ |
| D��ǿ��������ǿ��ԭ����ϲ�һ������������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com