
| A. | O2的摩尔质量是32g | B. | 氯化钠的相对原子质量是58.5g | ||
| C. | 1molH2O的质量是18g | D. | 1molH2O含有氢原子的个数2个 |
分析 A.摩尔质量的单位错误,应该为g/mol;
B.g为质量的单位,相对原子质量和相对分子质量都没有单位;
C.根据m=nM计算出水的质量;
D.1mol水分子中含有2mol氢原子,根据N=nNA计算出含有的氢原子数.
解答 解:A.O2的摩尔质量是32g/mol,故A错误;
B.氯化钠的相对分子质量为58.5,故B错误;
C.1mol水的质量为:18g/mol×1mol=18g,故C正确;
D.1molH2O含有2molH原子,含有氢原子数为2NA,故D错误;
故选C.
点评 本题考查了物质的量的应用,题目难度不大,明确摩尔质量与质量、相对分子量之间的关系为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,由分子式为C4H8的烯烃进行醛化反应,得到醛的同分异构体的数目为( )
,由分子式为C4H8的烯烃进行醛化反应,得到醛的同分异构体的数目为( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
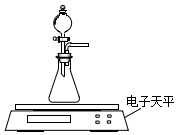 碳酸钙、盐酸是中学化学实验中的常用试剂.
碳酸钙、盐酸是中学化学实验中的常用试剂.| 物理量 实验序号 | V(0.1mol•L-1 HCl)/mL | m(颗粒状CaCO3)/g | m(粉末状CaCO3)/g | V(蒸馏水)/mL | ⑤ | ⑥ |
| 实验1 | a | b | 0 | c | d | |
| 实验2 | ① | 0 | ③ | c | d | |
| 实验3 | c | ② | 0 | ④ | d |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
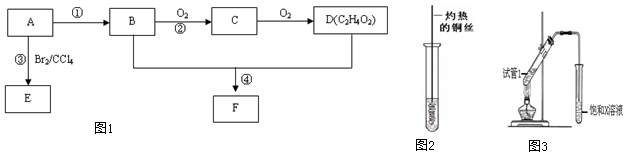
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 清晨的阳光穿过茂密的林木枝叶所产生的美丽的光线 | |
| B. | 向FeCl3溶液中滴加NaOH溶液出现红褐色沉淀 | |
| C. | 肾功能衰竭等疾病引起的尿中毒,可利用半透膜进行血液透析 | |
| D. | 在海水与河水交界处,易形成三角洲 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔质量为17 g•mol-1 | |
| B. | 所含的分子数目约为9.03×1023 | |
| C. | 在标准状况下体积约为33.6L | |
| D. | 溶于水制成0.5L溶液时物质的量浓度为1.5mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com