
用含杂质(杂质不与酸作用,也不溶于水)的铁10克与50克稀硫酸完全反应后,滤去杂质,所得液体质量为55.4克,求此铁的纯度。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
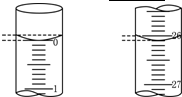 某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定 次数 |
待测氢氧化钠溶液的体积/mL | 0.1000 mol/L盐酸的体积(mL) | |
| 滴定前刻度 | 定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
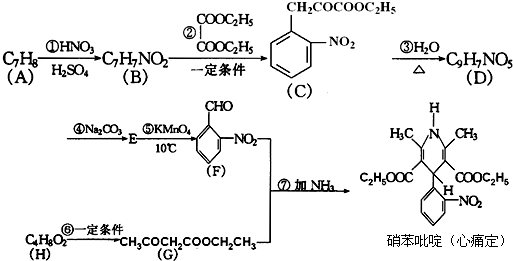
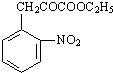 +H2O
+H2O
| ||
| △ |
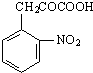 +C2H5OH
+C2H5OH +H2O
+H2O
| ||
| △ |
 +C2H5OH
+C2H5OH| 一定条件下 |
| 一定条件下 |
| ||
| 1000G |
| W总 |
| 10 |
| ||
| 1000G |
| W总 |
| 10 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 80(V2-V1)c |
| W |
| 80(V2-V1)c |
| W |
查看答案和解析>>
科目:高中化学 来源:辽宁省锦州市2010-2011学年度高二第一学期期末考试化学试题 题型:058
某学生用已知物质的量浓度的盐酸来滴定未知物质的量浓度的氢氧化钠
溶液时,选择酚酞作指示剂.请填写下列空白:
(1)配制待测液:用5.0 g含有少量杂质(杂质不与盐酸反应)的固体烧碱样品配制
1000 mL溶液.除烧杯和玻璃棒外,还需要的玻璃仪器有________、________.
(2)滴定:用标准的盐酸溶液滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,直到因加入一滴盐酸后,溶液由红色变为无色,并且半分钟内不恢复红色为止.读数:若滴定开始和结束时,酸式滴定管中的液面如下图所示,则起始读数为________mL,终点读数________mL.

(3)数据处理:某学生根据三次实验分别记录有关数据如下:

请选用其中合理的数据列式计算该氢氧化钠溶液的物质的量浓度:
c(NaOH)=________.
(4)误差讨论:(选填“偏高”、“偏低”或“无影响”)
①若酸式滴定管尖嘴部分滴定前无气泡,滴定终了有气泡,测得的氢氧化钠溶液的浓度将________.
②若改用含Na2O杂质的NaOH配制成标准溶液来滴定盐酸,测得的盐酸浓度将________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com