
| A. | 碱:苛性钠、纯碱、熟石灰 | |
| B. | 盐:胆矾、小苏打、铜绿 | |
| C. | 碱性氧化物:氧化铜、七氧化二锰、氧化铝 | |
| D. | 无丁达尔现象的分散系:碘的四氧化碳溶液、淀粉溶液、氯化铁溶液 |
分析 A.碱是指在电离时产生的阴离子全部是氢氧根离子的化合物;
B.离生成金属阳离子(或铵根离子)和酸根离子的化合物叫做盐;
C.和酸反应只生成盐和水的氧化物是碱性氧化物;
D.发生丁达尔现象的分散系是胶体,只需判断选项中分散系是否是胶体即可.
解答 解:A.纯碱为钠离子和碳酸根离子构成的盐,不属于碱,故A错误;
B.胆矾是五水硫酸铜的俗称,属于盐,小苏打为碳酸氢钠,为钠离子和碳酸氢根离子构成的盐,铜绿是碱式碳酸铜的俗称,属于盐,故B正确;
C.氧化铜属于碱性氧化物,Mn2O7和碱反应生成盐和水,如:Mn2O7+2KOH=2KMnO4+H2O,属于酸性氧化物,氧化铝属于两性氧化物,故C错误;
D.碘的四氯化碳溶液、氯化铁溶液都不是胶体,不会发生丁达尔现象,故D错误;
故选B.
点评 本题主要考查了物质的分类,掌握相关的概念以及胶体的性质等知识是解答的关键,平时注意相关知识的积累,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 电子式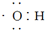 可以表示羟基,也可以表示氢氧根离子 可以表示羟基,也可以表示氢氧根离子 | |
| B. | 比例模型  可以表示二氧化碳分子,也可以表示水分子 可以表示二氧化碳分子,也可以表示水分子 | |
| C. | 明矾能水解生成Al(OH)3胶体,可用作饮用水杀菌 | |
| D. | 原子结构示意图 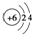 可以表示12C,也可以表示14C 可以表示12C,也可以表示14C |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
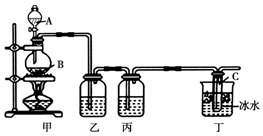 某化学活动小组欲用如图所示装置进行实验制取漂白液(次氯酸钠和氯化钠的混合溶液),并提高次氯酸钠含量.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2和NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3)试回答:
某化学活动小组欲用如图所示装置进行实验制取漂白液(次氯酸钠和氯化钠的混合溶液),并提高次氯酸钠含量.图中瓶乙盛饱和食盐水,瓶丙盛浓硫酸,分液漏斗A中盛浓盐酸.(据资料显示:Cl2和NaOH在不同温度下,产物不同.在较高温度下易生成NaClO3)试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从1 L 1 mol/L的NaCl溶液中取出10 mL,其浓度仍是1 mol/L | |
| B. | 10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8% | |
| C. | 0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数约为3×6.02×1023 | |
| D. | 配制0.5 L 10 mol/L的盐酸,需要标准状况下的氯化氢气体112 L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
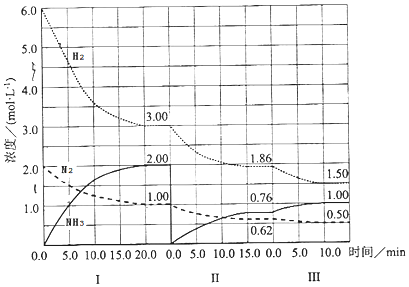
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 复分解反应 | B. | 化合反应 | C. | 离子反应 | D. | 氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用滴定管前要检查是否漏液 | |
| B. | 用简易量热计测定反应热时,用环形玻璃搅拌棒进行搅拌使酸和碱充分反应,以达到良好的实验效果 | |
| C. | 用精密pH试纸测得某浓度氯水的pH为3.5 | |
| D. | 燃料电池实验中,用KNO3溶液或Na2SO4溶液代替蒸馏水,效果要好得多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com