
| A. | 将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 | |
| B. | 将氯化铁饱和溶液煮沸,以制取氢氧化铁胶体 | |
| C. | 某无色溶液中加入足量稀盐酸无明显现象,再滴加BaCl2溶液有白色沉淀生成,则原溶液中一定含有SO42- | |
| D. | 用无锈铁丝蘸取某溶液在酒精灯上灼烧,火焰呈黄色,则说明该溶液中一定不含钾离子 |
分析 A.乙醇与水互溶;
B.氯化铁饱和溶液煮沸,铁离子浓度较大,水解生成沉淀;
C.加入足量稀盐酸无明显现象,排除银离子等干扰,再滴加BaCl2溶液有白色沉淀生成,白色沉淀为硫酸钡;
D.观察K的焰色反应应透过蓝色的钴玻璃.
解答 解:A.乙醇与水互溶,不分层,不能萃取碘水中的碘,故A错误;
B.氯化铁饱和溶液煮沸生成沉淀,应将小烧杯中蒸馏水加至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至溶液呈红褐色,停止加热制备胶体,故B错误;
C.加入足量稀盐酸无明显现象,排除银离子等干扰,再滴加BaCl2溶液有白色沉淀生成,白色沉淀为硫酸钡,则原溶液中一定含有SO42-,故C正确;
D.观察K的焰色反应应透过蓝色的钴玻璃,则该实验火焰呈黄色,可说明该溶液中一定含钠离子,不能确定是否含钾离子,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、胶体制备、离子检验及焰色反应等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的综合考查,注意实验的评价性分析,题目难度中等.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:解答题
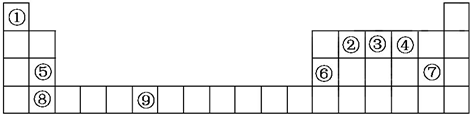
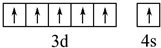 .
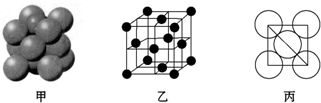
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,8g CH4含有4NA个氢原子 | |
| B. | 1mol Cu与足量FeCl3溶液反应,转移2NA个电子 | |
| C. | 1L0.1 mol•L-1(NH4)2SO4溶液中含有0.2NA个NH4+ | |
| D. | 10 L pH=l的硫酸溶液中含有的H+离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{8}^{18}$O2是${\;}_{8}^{16}$O2的同分异构体 | |
| B. | ${\;}_{8}^{18}$O2是O3的一种同素异形体 | |
| C. | ${\;}_{8}^{18}$O2与${\;}_{8}^{16}$O2互为同位素 | |
| D. | 1mol ${\;}_{8}^{18}$O2分子中含有20mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
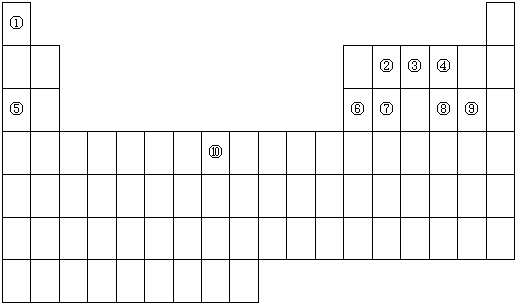
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×108 | 4.9×10-10 | K1=4.3×10-7 K1=5.6×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,46g有机物C2H6O中含有极性键的数目一定为7NA | |
| B. | 标准状况下,22.4L四氯化碳中所含有的Cl原子数目为4NA | |
| C. | 标准状况下,22.4升H2O中所含分子数大于NA | |
| D. | 常温常压下,33.6L氯气与56 g铁充分反应,转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com