
����Ŀ��SO2����Ϊ��ɫ���壬��ǿ�Ҵ̼�����ζ��������Ҫ��Ⱦ��֮һ��ijѧϰС��Ϊ��̽�����������ijЩ���ʣ�����������ʵ�顣
I.����ͼ��ʾ��ʹ��ҩƷ��װ��һ̽����������Ļ�ԭ��:
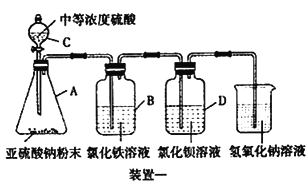
��1��װ��C������Ϊ________��
��2��B����Һ������Ϊ________��
��3��ѧ����Ԥ��װ��D ��û�а�ɫ���������������ŷ�Ӧ�Ľ��У�����D �в�����������ɫ������ѧ���Ҿ����������Ϸ���������ɫ�������������ᱵ����Ϊװ�û���Һ������������������������Ӧ����д��װ��D �еķ�Ӧ����ʽ________��
II.����˼�������������װ�ö����������Ƶ���Һ��ʹ����������ˮ������SO2 ����������ʱ���Ƿ����Ȼ�����Ӧ���ɳ�����
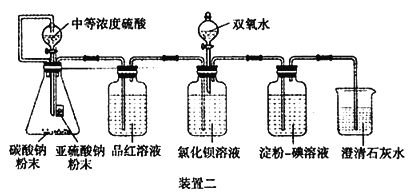
��4��̼���Ʒ�ĩ��Ŀ����________��
��5����______ʱ���Ȼ�����Һ��û�г������֣�˵�������������Ȼ�����Һ��Ӧ����ʱ�μ�˫��ˮ�������˰�ɫ������
��6���b�ö�ѡ�ó���ʯ��ˮ����������������Һ��Ŀ����________��
���𰸡� ��Һ©�� ��Һ���ػ�ɫ��Ϊdz��ɫ 2SO2+O2+2BaCl2+2H2O=2BaSO��+4HCl ����������̼,�ų�װ���е����� ������-����Һ��ɫ��ȥ(ֻ���Ʒ����ɫ������) ���������̼�Ƿ����ž�װ���еĿ���(�����ʯ��ˮ�����,֤��װ���п�����ȫ���ϳ������������𰸸���,ֻ�����ȥ�����SO2������)
����������1��װ��CΪ��Һ©����
��2��A�����ɶ��������������B�У���������Ὣ�Ȼ�����ԭΪ�Ȼ����������Կ���������Ϊ��Һ���ػ�ɫ��Ϊdz��ɫ��
��3����Ŀ��Ϊ�ǣ�װ�û���Һ������������������������Ӧ����һ����������+4��S����Ϊ+6�ۣ���Ӧ��һ����SO2��O2��BaCl2��������һ�������ᱵ��������ôClԪ��ֻ����HCl����ʽ���ڣ����Է�ӦΪ��Ҫ����H2O�����Է�ӦΪ2SO2 + O2 + 2BaCl2 + 2H2O = 2BaSO4��+ 4HCl��
��4��װ����Ҫ�ų�������������̼���ƺ����ᷴӦ�����ɵĶ�����̼���ſ�����
��5��������-����Һ��ɫ��ȥʱ��˵�����������Ѿ��������-����Һ�������Ȼ�����������˵�������������Ȼ�����Һ��Ӧ��ע�⣺��Ʒ����ɫ�Dz������ģ���Ϊ���ܶ����������ʹƷ����ɫ����δ�����Ȼ�����Һ��
��6����������������Һ����Ҫ������ָʾװ�õĿ����Ѿ��������ˣ�����������������Һ�л��ǣ�����������̼�����Ѿ����������ձ��У�װ���еĿ������ž���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�����pH=12��Ba��OH��2��Һ�У���μ���һ�����ʵ���Ũ�ȵ�NaHSO4��Һ������Һ�е�Ba2+ǡ����ȫ����ʱ����ҺpH=11������Ӧ����Һ���������Ba��OH��2��Һ��NaHSO4��Һ�����֮�ͣ���Ba��OH��2��Һ��NaHSO4��Һ������ǣ� ��
A.1�� 9
B.1��1
C.1��2
D.1��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������10mL 0.1 molL��1NaOH��Һ�м���0.1molL��1��һԪ��HA��ҺpH�ı仯������ͼ��ʾ������˵����ȷ���ǣ� �� 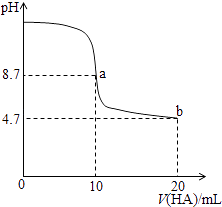
A.a����ʾ��Һ��c��Na+����c��A������c��H+����c��HA��
B.a��b������ʾ��Һ��ˮ�ĵ���̶���ͬ
C.pH=7ʱ��c��Na+��=c��A����+c��HA��
D.b����ʾ��Һ��c��A������c��HA��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺
��1��������ˮ�����������»�����������ɫ����Ϊ_______(�ѧʽ)��
��2����������ò����Լ�ƿʢװ����������Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______��
��3��ʵ���ҳ���Al2(SO4)3��NH3��H2O�Ʊ�Al(OH)3�䷴Ӧ�����ӷ���ʽΪ_______��
��4���ò�����պŨ������ڻ���ϣ����ڣ�Ũ������ֳ���������Ϊ_______��
��5��ά����C�ܽ�������ȡ��Fe3+ת��ΪFe2+,˵��ά����C����_______(ѡ������������������ԭ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܴ���Mg2+��Fe2+��Fe3+ �� ����NaOH��Һ����ʼʱ�а�ɫ��״�������ɣ���ɫ����Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ�����н�����ȷ���ǣ� �� 
A.һ����Fe2+ �� һ��û��Fe3+��Mg2+
B.һ����Fe3+ �� һ��û��Fe2+��Mg2+
C.һ����Fe3+ �� ������Fe2+ �� һ��û��Mg2+
D.һ����Fe2+ �� ������Mg2+ �� һ��û��Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ������������ԭ��Ӧ����
A. Fe��CuSO4===FeSO4��Cu B. NH4HCO3![]() NH3����H2O��CO2��
NH3����H2O��CO2��
C. Cl2��H2O![]() HCl��HClO D. Fe2O3��3CO
HCl��HClO D. Fe2O3��3CO![]() 2Fe��3CO2
2Fe��3CO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��3mol��Ȳ��5mol�������ܱ������з�Ӧ������ﵽƽ��ʱ������amol��ϩ����ƽ����������ȫȼ������CO2��H2O���������������ʵ����ǣ�������
A.6mol
B.10mol
C.3amol
D.3mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ����������ͺ�����ͬ��ͬѹ�¾�����ͬ�ģ� ��
A.ԭ����B.���C.������D.����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com