
【题目】近日IPCC发布了由来自40个国家的91位科学家编写的《全球升温1.5℃特别报告》,温室效应引发的环境问题日益严重,物种灭绝,洪灾、旱灾、粮食欠收等自然灾害发生频率不断增加,CO2的减排和综合利用是解决温室及能源问题的有效途径。
(1)CO2可转化成有机物实现碳循环。在体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如图所示。
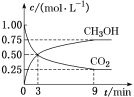
① 从3 min到9 min,v(H2)=_____mol·L-1·min-1。
② 该反应的平衡常数为_______。
③ 下列说法正确的的是____(填字母)。
A.混合气体的密度不随时间的变化而变化,则说明上述反应达到平衡状态
B.平衡时CO2的转化率为75%
C.平衡时混合气体中CH3OH(g)的体积分数是30%
D.该条件下,第9 min时v逆(CH3OH)大于第3 min时v正(CH3OH)。
(2)工业中,CO2和H2在催化剂Cu/ZnO作用下可发生两个平行反应,分别生成CH3OH和CO。
反应A:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
反应B:CO2(g)+H2(g)![]() CO(g)+H2O(g)
CO(g)+H2O(g)
控制CO2和H2初始投料比为1∶3时,温度对CO2平衡转化率及甲醇和CO产率的影响如图所示。
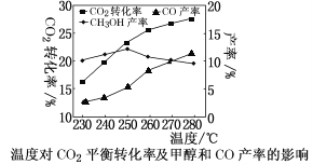
① 由图可知温度升高CO的产率上升,其主要原因可能是________。
② 由图可知获取CH3OH最适宜的温度是________。下列措施有利于提高CO2转化为CH3OH的平衡转化率的有___________(填字母)。
A.使用催化剂 B.增大体系压强
C.增大CO2和H2的初始投料比 D.投料比不变和容器体积不变,增加反应物的浓度
(3)250 ℃下CH3OH物质的量随时间的变化曲线如图所示。画出280 ℃下0~t2时刻CH3OH物质的量随时间的变化曲线示意图__________。
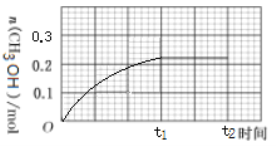
【答案】0.125 5.3 B C 反应B是吸热反应 250℃ B D 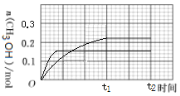
【解析】
(1)①3min到9min,根据CO2浓度变化计算CO2化学反应速率,利用计量数之比得到υ(H2);②结合各物质的平衡浓度,利用三段式法计算该反应的平衡常数;③A.该反应过程中密度为定值;B.根据二氧化碳的转化率=![]() ×100%计算平衡时CO2的转化率;C.平衡时混合气体中CH3OH(g)的体积分数等于平衡时甲醇的物质的量浓度与其它物质总物质的量浓度的百分比;D.该反应从开始至达到平衡状态,正反应速率逐渐减小,逆反应速率逐渐增大;
×100%计算平衡时CO2的转化率;C.平衡时混合气体中CH3OH(g)的体积分数等于平衡时甲醇的物质的量浓度与其它物质总物质的量浓度的百分比;D.该反应从开始至达到平衡状态,正反应速率逐渐减小,逆反应速率逐渐增大;
(2)①反应B正反应是吸热反应,温度升高平衡正向移动,CO产率升高;②据图示进行分析温度与甲醇转化率的关系;由CO2(g)+3H2(g)CH3OH(g)+H2O(g) 可知提高CO2转化为CH3OH平衡转化率,应使平衡向正向移动,可增大压强,增大浓度;
(3)根据温度对反应速率及化学平衡的影响分析。
(1)①3min到9min,CO2浓度变化为0.5mol/L-0.25mol/L=0.25mol/L,CO2反应速率=![]() =
=![]() mol/(Lmin),υ(H2)=3×υ(CO2)=0.125mol/(Lmin),故答案为:0.125;
mol/(Lmin),υ(H2)=3×υ(CO2)=0.125mol/(Lmin),故答案为:0.125;
② CO2(g) + 3H2(g)CH3OH(g)+H2O(g)
起始(mol/L) 1 3 0 0
转化(mol/L) 0.75 2.25 0.75 0.75
平衡(mol/L) 0.25 0.75 0.75 0.75
该反应的平衡常数K=![]() ≈5.3,故答案为:5.3;
≈5.3,故答案为:5.3;
③A.该反应前后都是气体,气体总质量始终不变,容器容积不变,则密度为定值,不能根据密度判断平衡状态,故A错误;B.平衡时CO2的转化率=![]() ×100%=75%,故B正确;C.平衡时混合气体中CH3OH(g)的体积分数=
×100%=75%,故B正确;C.平衡时混合气体中CH3OH(g)的体积分数=![]() ×100%=30%,故C正确;D.从反应开始到平衡过程中正反应速率逐渐减小,直至达到平衡状态,则第9min时达到平衡状态υ逆(CH3OH)=υ正(CH3OH),则9min时υ逆(CH3OH)一定小于第3min时υ正(CH3OH),故D错误;故答案为:BC;
×100%=30%,故C正确;D.从反应开始到平衡过程中正反应速率逐渐减小,直至达到平衡状态,则第9min时达到平衡状态υ逆(CH3OH)=υ正(CH3OH),则9min时υ逆(CH3OH)一定小于第3min时υ正(CH3OH),故D错误;故答案为:BC;
(2)①由图示可知,温度升高CO的产率上升,其主要原因可能是反应B正反应是吸热反应,温度升高平衡正向移动,CO产率升高,故答案为:反应B正反应是吸热反应;
②据图示可知,250℃甲醇产率最高,故获取CH3OH最适宜的温度是250℃;A.使用催化剂,平衡不移动,不能提高转化率,故A错误;B.增大体系压强,平衡向正方向移动,提高CO2转化率,故B正确;C.增大CO2和H2的初始投料比,可增大氢气的转化率,二氧化碳的转化率减小,故C错误;D.投料比不变,增加反应物的浓度,相当于增大压强,平衡正向移动,可增大转化率,故D正确;故答案为:250℃;BD;
(3)温度升高,反应速率加快,则反应达到平衡的时间小于t1;280℃时甲醇的产率小于250℃时,所以达到平衡后,体系中甲醇的量变小,据此画出280℃下0~t2时刻CH3OH物质的量随时间的变化曲线: ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】某酸式盐NaHY的水溶液显碱性,下列叙述正确的是( )
A.H2Y的电离方程式为:H2Y![]() 2H++Y2-
2H++Y2-
B.HY-的水解方程式为:HY-+H2O![]() H3O++Y2-
H3O++Y2-
C.该酸式盐溶液中离子浓度关系为:c(Na+)>c(HY-)>c(OH-)>c(H+)>c(Y2-)
D.该酸式盐溶液中离子浓度关系为:c(Na+)>c(Y2-)>c(HY-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含非极性共价键,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径:W<X<Y<Z
B. 阴离子的还原性:Y>W
C. a—定由W、X两种元素组成
D. 图中转化过程d物质在作为反应物时均即为氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个绝热的恒容密闭容器中,可逆反应![]() 达到平衡状态的标志是( )
达到平衡状态的标志是( )
①![]() ②各组分的物质的量不变 ③体系的压强不再发生变化 ④混合气体的密度不变 ⑤体系的温度不再发生变化 ⑥
②各组分的物质的量不变 ③体系的压强不再发生变化 ④混合气体的密度不变 ⑤体系的温度不再发生变化 ⑥![]() ⑦3mol H-H键断裂的同时有2mol N-H键也断裂
⑦3mol H-H键断裂的同时有2mol N-H键也断裂
A.①②③⑤⑥B.②③④⑤⑥
C.②③⑤⑥D.②③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,浓度都是1mol·L-1的两种气体X2和Y2在密闭容器中反应,经过tmin后,测得物质的浓度分别为:c(X2)=0.4mol·L-1,c(Y2)=0.8mol·L-1,则该反应的方程式可表示为()
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知拆开1mo1H-H键、1molN≡N键、lmolN-H键分别需要吸收的能量为436kJ、946kJ、391kJ。则生成1mo1 NH3时反应放出___________kJ 的热量。
(2)为了验证Fe3+与Cu2+氧化性强弱,下列装置能达到实验目的的是________(填序号)。

(3)直接乙醇燃料电池(DEFC)具有很多优点,引起了人们的研究兴趣。现有以下三种乙醇燃料电池。

①三种乙醇燃料电池中正极反应物均为______________________;
②碱性乙醇燃料电池中,电极a上发生的电极反应式为_______________________________;
③熔融盐乙醇燃料电池中若选择熔融碳酸钾为介质,电池工作时,电极b上发生的电极反应式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化合物2苯基丙烯(![]() ),下列说法正确的是
),下列说法正确的是
A. 不能使稀高锰酸钾溶液褪色
B. 可以发生加成聚合反应
C. 分子中所有原子共平面
D. 易溶于水及甲苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
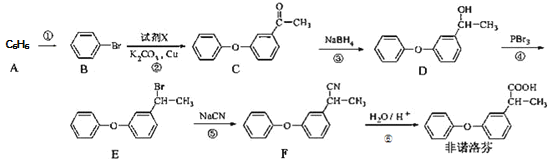
回答下列问题
(1)![]() 的化学名称是_____________,
的化学名称是_____________,![]() 中含氧官能团的名称为___________。
中含氧官能团的名称为___________。
(2)上述反应中,反应①的条件是___________,过程①属于______反应
(3)反应②发生的是取代反应,且另一种产物有![]() ,写出由
,写出由![]() 生成
生成![]() 的化学方程式______。
的化学方程式______。
(4)有机物![]() 与非诺芬互为同分异构体,
与非诺芬互为同分异构体,![]() 满足下列条件:
满足下列条件:
I.能与NaHCO3溶液反应,且能与FeCl3溶液发生显色反应
II.分子中有6种不同化学环境的氢,且分子中含有两个苯环
![]() 的结构有_____种,写出其中一种不能与浓溴水发生取代反应的
的结构有_____种,写出其中一种不能与浓溴水发生取代反应的![]() 的结构简式_________。
的结构简式_________。
(5)根据已有知识并结合相关信息,写出以![]() 为原料制备
为原料制备 路线流程图(无机试剂任用)_________
路线流程图(无机试剂任用)_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数,下列判断正确的是( )
A.22.4L氯气中含有的Cl数目为2NA
B.1.0mol/LCaCl2溶液中含有的Cl-数目为2NA
C.7.8gNa2O2晶体中含有的Na+数目为0.1NA
D.2.0g重水(2H216O)中含有的中子数目为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com