
| A. | 浓硫酸具有吸水性,因而能使蔗糖炭化 | |
| B. | 浓硫酸在常温下不容易与铜片反应放出二氧化硫气体 | |
| C. | 浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 | |
| D. | 浓硫酸在常温下能够使铁、铝、锌等金属钝化 |
分析 浓硫酸使蔗糖炭化,是利用了浓硫酸的脱水性;浓硫酸虽然具有氧化性,但和铜反应时需要加热;氨气是一种碱性气体,不能用浓硫酸来干燥,可以用碱石灰来干燥氨气.在浓硫酸中发生钝化的是铁和铝,据此分析.
解答 解:A.浓硫酸具有脱水性,可使蔗糖碳化,故A错误;
B.浓硫酸与铜的反应应在加热条件下进行,在常温下不容易反应,故B正确;
C.浓硫酸与氢气不反应,可用于干燥氢气,能与氨气反应所以不能用浓硫酸干燥,故C错误;
D.浓硫酸具有强氧化性,在常温下可使铁、铝等金属在表面生成一层致密的氧化膜而钝化,不能使Zn钝化,故D错误.
故选B.
点评 本题考查浓硫酸的性质,为高考高频考点,侧重于学生的基础知识的综合理解和运用的考查,注意把握浓硫酸的特性以及性质之间的区别,难度不大,注意相关基础的积累.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮肥厂用氢气和氮气合成氨 | |
| B. | 钢铁在潮湿空气中生锈 | |
| C. | 往硫酸铜晶体上滴入浓硫酸,颜色由蓝色变成白色 | |
| D. | 石油分馏后得汽油、煤油等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl→H2SO4→H2S→NaOH→CO2 | B. | NaCl→Na2SO4→NaOH→H2S→CO2 | ||
| C. | Na2S→Na2SO4→NaCl→NaOH→CO2 | D. | Na2SO4→HCl→H2S→NaOH→CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1.00 mol•L-1 | B. | 0.500 mol•L-1 | C. | 2.00 mol•L-1 | D. | 3.00 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
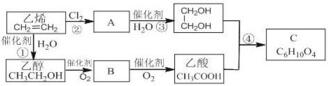
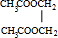 +2H2O.
+2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com