
������������ȷ���ǣ�������
��1��������̼�ظ�������
��2���ð�ˮ��ȥ�Թ��ϵ�����
��3�������������ά������̫���ܵ�ص���Ҫԭ��
��4������ϡ���ᡢ̼������Һ����������Һ���ʵ������֤Ԫ�صķǽ�����Cl��C��̼����Si
��5������ֻ�ܸı䷴Ӧ�Ļ�ܣ����ܸı䷴Ӧ����ЧӦ
��6����������̲������������������������跴Ӧ������
��7��ͬ����Ԫ�صļ������ӻ�ԭ��Խǿ��ˮ��̶�Խ��
��8��Al2O3�ڹ�ҵ�������������²��ϣ�Ҳ���ڵ�ⷨ������
��9�������ЧӦ������������Һ�뽺�壬�ơ������ܲ��������ЧӦ
��10������������ˮ��������ɱ����̼�ᱵ�����ڱ����ӣ�
| �� | A�� | ��1����4����6����7�� | B�� | ��4����6����9����10�� | C�� | ��3����5����6����8�� | D�� | ��5����6����8����9�� |
| ���Ļ�ѧ���ʣ��������Ҫ���ʣ����������ã����Ļ�ѧ���ʣ���Ͷ������裻þ��������Ҫ�����. | |
| ר�⣺ | Ԫ�ؼ��仯�����ѧӦ�ã� |
| ������ | ��1��̼�ظ������绯ѧ��ʴ�� ��2����ˮ����������Ӧ�� ��3���������̫���ܵ�أ� ��4�����ø����ᡢ̼������Һ����������Һ���ʵ������֤Ԫ�صķǽ�����Cl��C��̼����Si�� ��5������ֻ�ܸı䷴Ӧ�Ļ�ܣ����ܸı䷴Ӧ����ʼ������״̬�� ��6�����������������跴Ӧ�����ʾ�����;�� ��7����ԭ����ˮ��̶��أ� ��8��Al2O3���۵�ߣ�AlΪ���ý�������ⷨ�������� ��9�������ЧӦ�ǽ������е����ʣ� ��10������������ǿ�����ԣ�̼�ᱵ�������ᷴӦ�����ж��ı����ӣ� |
| ��� | �⣺��1��̼�ظ������绯ѧ��ʴ����������ʴ���ʴ��� ��2����ˮ����������Ӧ��Ӧ����ϡ������ϴ���ʴ��� ��3���������̫���ܵ�أ����������������ά���ʴ��� ��4�����ø����ᡢ̼������Һ����������Һ���ʵ������֤Ԫ�صķǽ�����Cl��C��̼����Si��������ӷ�������Ʒ�Ӧ���Ҳ�����������������ԱȽϷǽ����ԣ��ʴ��� ��5������ֻ�ܸı䷴Ӧ�Ļ�ܣ����ܸı䷴Ӧ����ʼ������״̬�����ܸı䷴Ӧ����ЧӦ������ȷ�� ��6�����������������跴Ӧ�����ʾ�����;������������̲���������ȷ�� ��7����ԭ����ˮ��̶��أ���±�������е����ӻ�ԭ��ǿ����������ˮ�⣬�ʴ��� ��8��Al2O3���۵�ߣ�Ϊ���ӻ����AlΪ���ý�������ⷨ��������Al2O3�ڹ�ҵ�������������²��ϣ�Ҳ���ڵ�ⷨ������������ȷ�� ��9�������ЧӦ�ǽ������е����ʣ����ЧӦ������������Һ�뽺�壬�ơ������ܲ��������ЧӦ������ȷ�� ��10������������ǿ�����ԣ���������ˮ��������ɱ����̼�ᱵ�������ᷴӦ�����ж��ı����ӣ�Ӧѡ���ᱵ���ڱ����ӣ��ʴ��� ��ѡD�� |
| ������ | ���⿼�����ʵ����ʣ�Ϊ��Ƶ���㣬���ճ���Ԫ�ػ�����֪ʶ����ѧ����Ϊ���Ĺؼ���ע����������;�Ĺ�ϵ��ע�ػ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ��� |


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д� ��ǰ�κ�ͬ����ϰϵ�д�
��ǰ�κ�ͬ����ϰϵ�д� ����С��ҵϵ�д�
����С��ҵϵ�д� �Ƹ�С״Ԫ����������ϰ��ϵ�д�
�Ƹ�С״Ԫ����������ϰ��ϵ�д� �ɹ�ѵ���ƻ�ϵ�д�
�ɹ�ѵ���ƻ�ϵ�д� ����ѵ����ֱͨ�п�����ϵ�д�
����ѵ����ֱͨ�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��0.10 mol CH3COONa�ӵ�1.0 L 0.10 mol��L��1 CH3COOH��Һ�У����CH3COONa��Һ������䣩������Һ��pH����֪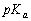 = 4.74����
= 4.74����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����йػ�ѧ�����ʾ����ȷ���� ( )
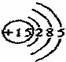 A��Pԭ�ӵĽṹʾ��ͼ��
A��Pԭ�ӵĽṹʾ��ͼ��
B��NaCl�ĵ���ʽΪ�� 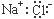
C��HCN���ӵĽṹʽ��H��C��N
D����78�����ӵĵ�ķ����Ժ��أ�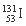
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��B��C��D����Ԫ�ض��Ƕ�����Ԫ�أ�AԪ�ص����Ӿ��л�ɫ����ɫ��Ӧ��BԪ�ص����ӽṹ��Ne������ͬ�ĵ��Ӳ��Ų���5.8 g B����������ǡ������100 mL 2 mol・L�D1������ȫ��Ӧ��Bԭ�Ӻ�������������������ȡ�H2��C������ȼ�ղ�����ɫ���档DԪ��ԭ�ӵĵ��Ӳ�ṹ�У������������Ǵ�����������3�����������������ش�
��1��Ԫ��Cλ�ڵ�__________���ڵ�__________�壬�������������Ļ�ѧʽΪ____________��
��2��AԪ����_________��BԪ����________��DԪ����_______���������ƣ�
��3��A��D�γ��ȶ�������ĵ���ʽ��_____________���жϸû������ڿ������Ƿ���ʵļ�����_______________________________��
��4��CԪ�صĵ����ж�������A������������Ӧ��ˮ�������Һ���գ������ӷ���ʽΪ___________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и���������ָ����Һ�й������ӹ����˵����ȷ���ǣ�������
| �� | A�� | 25��ʱ��Һ��һ���������棺Na+��Ca2+��Cl����SO42�� |
| �� | B�� | ��������Ӧ�ų���������Һ��һ�����棺Mg2+��Cu2+��SO42����NO3�� |
| �� | C�� | ��������Һ�п��ܴ������棺Na+��K+��Cl‾��HCO3‾ |
| �� | D�� | 0.1mol/LFeCl3��Һ�п��ܴ������棺Fe2+��NH4+��SCN����SO42�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
a molNa2O2��b molNaHCO3�����Ϻ����ܱ������м��ȵ�250�棬ʹ���ַ�Ӧ�����ų�����Ϊ��������ʱ��a��b������Ϊ��������
| �� | A�� | 3��4 | B�� | 4��5 | C�� | 2��3 | D�� | 3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ��װ�ý�����Ӧʵ�飬�ܴﵽʵ��Ŀ�ĵ���
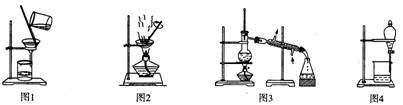
A����ͼ1��ʾװ�ô�Fe(OH)3�����й��˳�Fe(OH)3����
B����ͼ2��ʾװ��������CuCl2��Һ�в���ˮ�Ƶ�CuCl2��2H20����
C����ͼ3��ʾװ�ô�CH3OH��C2H5OH�Ļ�����з�����Ҵ�
D����ͼ4��ʾװ�ô�C2H5OH��C2H5OOCCH3�Ļ�����з������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ƶ���ȷ����
A����H+(aq)+OH-(aq)=H20��1�� ��H=-57��3 kJ��mol-1����֪��1 mo1 CH3COOH����Һ�뺬1 mol NaOH����Һ��ϣ��ų�����Ϊ57��3 kJ
B����C(ʯī)=C(���ʯ) ��H=+1��9 kJ��mol-1����֪ʯī�Ƚ��ʯ���ȶ�
C����N2(g)+3H2(g)=2NH3(g) ��H=-92��4 kJ��mol-1����֪��1 mol N2(g)��3 mol H2(g)�����ܱ������г�ַ�Ӧ��ų�����Ϊ92��4 kJ
D���ɡ�G����H-T��S��֪�����еķ��ȷ�Ӧ�����Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����
A������մ�����ϣ�Ӧ������NaOH��Һ��ϴ
B�����Թ���Һ�����ʱ��Һ�岻�����Թ��ݻ���1/3
C����NaOH��Һ����μ�����������FeCl3��Һ�����Ƶ�Fe��OH��3����
D���Թܱ��ϵ���������ϡ����ϴ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com