
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
| 微粒 | ClO- | ClO2- | ClO3- | ClO4- |
| 立体结构 |
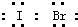
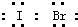
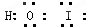
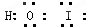
查看答案和解析>>
科目:高中化学 来源:学习高手选修化学(物质结构与性质人教版) 人教版 题型:022
ClO-、ClO![]() 、ClO
、ClO![]() 、ClO
、ClO![]() 、中、Cl都是以sp3杂化轨道与O成键,则ClO-是形,ClO
、中、Cl都是以sp3杂化轨道与O成键,则ClO-是形,ClO![]() 是________形,ClO
是________形,ClO![]() 是________形,ClO
是________形,ClO![]() 是________形离子构型.
是________形离子构型.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2014届福建三明泰宁一中高二下第一次阶段考试化学试卷(解析版) 题型:填空题
Ⅰ.请按下列要求写出相应粒子的电子排布式,并回答有关问题:
⑴写出基态原子或离子的电子排布式:
①Fe3+_________________; ②Cr _______________; ③Cu _______________.
⑵比较 Fe2+与Fe3+的化学稳定性:Fe2+ Fe3+,半径大小:Fe2+ Fe3+
Ⅱ⑴在第三周期中,第一电离能最小的元素是________,电负性最大的元素是________(用元素符号表示)。
⑵第二、三、周期原子中p轨道半充满的元素是_______ (用元素符号表示)。
⑶第二周期原子中,未成对电子数等于周期系数的原子有 (用元素符号表示)
Ⅲ. (2010·滁州模拟)ClO、ClO、ClO中Cl都是以sp3杂化轨道与O原子成键的,试推测下列微粒的立体结构。
|
微粒 |
ClO |
ClO |
ClO |
|
立体结构 |
|
|
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com