
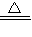 CuSO4+SO2��+2H2O
CuSO4+SO2��+2H2O 2CuSO4+2H2O�ӷ�Ӧ����ʽ����������������;�������������٣�;���ܲ��������Ⱦ���������壬
2CuSO4+2H2O�ӷ�Ӧ����ʽ����������������;�������������٣�;���ܲ��������Ⱦ���������壬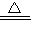 CuSO4+SO2��+2H2O���ӷ�Ӧ����ʽ���������������+6�۱�Ϊ�����е�+4��������ǿ�����ԣ��������ᷴӦ�������Σ���������������ԣ�;���ܵķ�Ӧ��2Cu+O2+2H2SO4��ϡ��
CuSO4+SO2��+2H2O���ӷ�Ӧ����ʽ���������������+6�۱�Ϊ�����е�+4��������ǿ�����ԣ��������ᷴӦ�������Σ���������������ԣ�;���ܵķ�Ӧ��2Cu+O2+2H2SO4��ϡ�� 2CuSO4+2H2O�ij����ӷ�ӦΪ2Cu+O2+4H+=2Cu2++2H2O��
2CuSO4+2H2O�ij����ӷ�ӦΪ2Cu+O2+4H+=2Cu2++2H2O��

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| +4 |
| S |
| +6 |
| S |
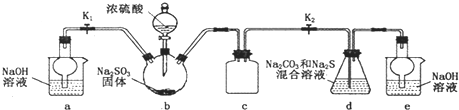
| 3.16nv |
| m |
| 3.16nv |
| m |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
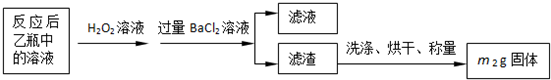
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
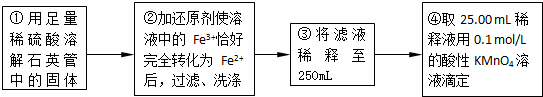
| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ����KMnO4��Һ���/mL | 25.00 | 25.03 | 24.97 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 7(W2-W1) |
| a |
| 7(W2-W1) |
| a |
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
6![]() +10Al+18H2O
+10Al+18H2O![]() 3N2��+10Al(OH)3+6OH-
3N2��+10Al(OH)3+6OH-
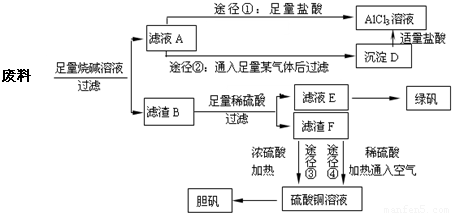
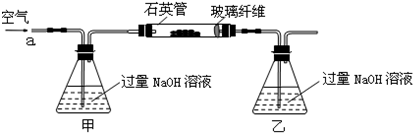
ij��ѧ��ȤС���ͬѧ����̽�����ֻ�������;����
��1������þ�����ܸ�������������Ⱦ���䷴Ӧԭ���ͽ�������ͬ������þ���ɺ�ˮ����ȡ��MgCl2ͨ������Ƶõġ���Ҫ��ȥ1 m3��ˮ��0.3 mol��![]() ����������Ҫ��0.5%������������MgCl2�ĺ�ˮ����ǧ�ˣ�
����������Ҫ��0.5%������������MgCl2�ĺ�ˮ����ǧ�ˣ�
��2�����״����뺬![]() �ķ�ˮ��Ҳ������������Ⱦ��������һ�����������·�����Ӧ��
�ķ�ˮ��Ҳ������������Ⱦ��������һ�����������·�����Ӧ��
6![]() +6H++5CH3OH
+6H++5CH3OH![]() 3N2��+5CO2��+13H2O
3N2��+5CO2��+13H2O
��ij��ˮ��������������ʱ��![]()
![]() N2��ת����Ϊa%����ôÿ�촦���˺�
N2��ת����Ϊa%����ôÿ�촦���˺�![]() Ϊb g��L-1�ķ�ˮV m3���ܶ�1 g��cm-3������Ҫ�״�����ǧ�ˣ���Ҫ��д�����ⲽ�裬��������е����ݼ������ֻ��д������ʽ�����ػ���
Ϊb g��L-1�ķ�ˮV m3���ܶ�1 g��cm-3������Ҫ�״�����ǧ�ˣ���Ҫ��д�����ⲽ�裬��������е����ݼ������ֻ��д������ʽ�����ػ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com