
【题目】铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题: 
(1)生铁中含有一种铁碳化合物X(Fe3C).X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是 .
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是;
A.Mg2+
B.Fe2+
C.Al3+
D.Cu2+
(3)氧化铁是重要工业颜料,用废铁屑制备它的流程如图:回答下列问题: ①操作Ⅰ的名称是 , 操作Ⅱ的名称是 .
②写出在空气中煅烧FeCO3的化学方程式;
(4)有些同学认为KMnO4溶液可以测定亚铁离子含量(5Fe2++MnO4﹣+8H+═5Fe3++Mn2++4H2O). a.称取2.850g绿矾(FeSO47H2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL所配溶液于锥形瓶中;
c.加入20.00mL硫酸酸化的0.01mol/LKMnO4溶液恰好完全反应.
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需 . 定容时俯视刻度线,则c(KMnO4)(填偏大、偏小或不变)
②计算上述样品中FeSO47H2O的质量分数为 .
【答案】
(1)Fe2+、Fe3+、H+
(2)BC
(3)过滤;洗涤;4FeCO3+O2 ![]() 2Fe2O3+4CO2
2Fe2O3+4CO2
(4)250 mL容量瓶;偏大;0.975
【解析】解:(1)Fe3C在足量的空气中高温煅烧,生成有磁性的固体Y,Y为Fe3O4 , 溶于过量的盐酸反应生成氯化亚铁、氯化铁,溶液有剩余的HCl,溶液中大量存在的阳离子是Fe2+、Fe3+、H+ , 所以答案是:Fe2+、Fe3+、H+;(2)加入过量的NaOH,Al3+转化为偏铝酸根,Mg2+、Fe2+、Cu2+转化为氢氧化物沉淀,且氢氧化亚铁易被氧化,灼烧固体得到氧化镁、氧化镁、氧化铁,用过量的稀盐酸中,所得溶液中含有Mg2+、Fe3+、Cu2+ , 与原溶液相比,溶液中大量减少的阳离子是Al3+、Fe2+ , 所以答案是:BC;(3)①由工艺流程可知,操作I是将固体与液体分离,应采取过滤的方法;FeCO3沉淀会附着其它离子,需要进行洗涤,减少杂质,所以答案是:过滤;洗涤;②在空气中煅烧FeCO3的化学方程式为4FeCO3+O2 ![]() 2Fe2O3+4CO2 , 所以答案是:4FeCO3+O2
2Fe2O3+4CO2 , 所以答案是:4FeCO3+O2 ![]() 2Fe2O3+4CO2;(4)①精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需250 mL容量瓶,定容时俯视刻度线,体积偏小,由c=
2Fe2O3+4CO2;(4)①精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需250 mL容量瓶,定容时俯视刻度线,体积偏小,由c= ![]() 可知,c偏大,所以答案是:250mL容量瓶;偏大;②n(MnO4﹣)=0.01000mol/L×0.02L=2×10﹣4mol,则由5Fe2++MnO4﹣+8H+═5Fe3++Mn2++4H2O可知n(Fe2+)=5×2×10﹣4mol=1×10﹣3mol, 所以250mL溶液中含有知n(Fe2+)=1×10﹣2mol,则m(FeSO47H2O)=278g/mol×1×10﹣2mol=2.780g,样品中FeSO47H2O的质量分数为
可知,c偏大,所以答案是:250mL容量瓶;偏大;②n(MnO4﹣)=0.01000mol/L×0.02L=2×10﹣4mol,则由5Fe2++MnO4﹣+8H+═5Fe3++Mn2++4H2O可知n(Fe2+)=5×2×10﹣4mol=1×10﹣3mol, 所以250mL溶液中含有知n(Fe2+)=1×10﹣2mol,则m(FeSO47H2O)=278g/mol×1×10﹣2mol=2.780g,样品中FeSO47H2O的质量分数为 ![]() =0.975,所以答案是:0.975.
=0.975,所以答案是:0.975.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
【题目】元素X、Y、Z、M、N均为原子序数依次增大的短周期主族元素;R在地壳金属元素中的含量仅次于Z。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3:4;N-、Z3+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)R在元素周期表中的位置是____________;Z3+的离子结构示意图是____________。
(2)写出X、Y、N按原子个数之比1:1:1:形成的化合物的电子式__________;M和N气态氢化物的稳定性大小比较为________(用化学式和“>”“<”或“=”表示)。
(3)X与Y可分别形成10电子和18电子的分子,写出该18电子分子转化成10电子分子的化学方程式__________________________________.
(4)Z元素的单质能与Y和R形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_____________________________。
(5)下图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,在该转化关系中还原剂是__________(填化学式),示意图中转移电子的数目为______。


(6)由X、Y、M三种元素组成的离子,在水溶液中与H+和OH-均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )
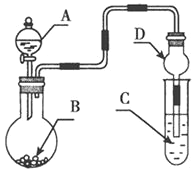
A. 若A为H2O2,B为MnO2,C中盛有Na2S溶液,C中溶液变浑浊
B. 若A为浓盐酸,B为MnO2,C中盛有KI-淀粉溶液,C中溶液变蓝色
C. 若A为浓氨水,B为生石灰,C中盛有AlCl 3溶液, C中先产生白色沉淀后沉淀又溶解
D. 若A为浓盐酸 ,B为CaCO3,C中盛有Na2SiO3溶液,C中溶液出现白色沉淀,证明非金属性Cl>C>Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为FeO和CuO的混合物,取两份等质量的X样品进行下列实验:设第3步所得固体D的质量为 32g,溶液E中只含有一种金属离子,气体F在标准状况下体积为5.6 L,则X中FeO与CuO的物质的 量之比为( ) 
A.4:1
B.1:2
C.2:1
D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的焓变,并采取相应措施。化学反应的焓变通常用实验进行测定,也可进行理论推算。
(1)实验测得,5g甲醇(CH3OH 液态)在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5kJ的热量,试写出甲醇燃烧的热化学方程式:________________。
(2)下图是某笔记本电脑用甲醇燃料电池的结构示意图。
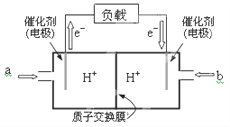
放电时甲醇应从______处通入(填“a”或“b”),电池内部H+向_____(填“左”或“右”)移动。写出电池负极的电极反应式:_______________________________。
(3)由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
化学键 | H-H | N-H | N≡N |
键能/kJ·mol-1 | 436 | a | 945 |
已知反应N2(g)+3H2(g)![]() 2NH3(g) △H=-93 kJ·mol-1。试根据表中所列键能数据计算a 的数值:_______________。
2NH3(g) △H=-93 kJ·mol-1。试根据表中所列键能数据计算a 的数值:_______________。
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算。
已知:C(s,石墨)+O2(g)=CO2(g) △H1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) △H2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) △H3=-2599kJ·mol-1
根据盖斯定律,计算2C(s,石墨)+H2(g)=C2H2(g)反应的焓变△H =________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜和镁的合金4.6g完全溶于浓硝酸,若反应中硝酸被还原只产生4480mL的NO2气体和336mL的N2O4气体(都已折算到标准状况),在反应后的溶液中,加入足量的NaOH溶液,生成沉淀的质量为多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C11H12O5)同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只有2种;③1 mol A与足量的NaHCO3反应生成1 mol CO2;④遇FeCl3溶液不显色。A有如图所示转化关系:
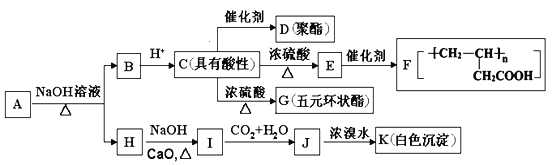
已知: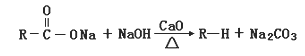
回答下列问题:
(1)E中官能团名称_____________________,H的分子式为_____________________。
(2)由C生成G的反应类型是____________________。
(3)A的结构简式为_____________________,G的结构简式为___________________。
(4)①写出C→D反应的化学方程式__________________________________________;
②写出I→J反应的离子方程式__________________________________________。
(5)C的同分异构体中能同时满足下列条件:a.能发生银镜反应,b.能发生皂化反应;c.能与Na反应产生H2,共有__________种(不含立体异构)。其中核磁共振氢谱显示为3组峰,且峰面积比为6∶1∶1的是_________________________(写结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸雨给人类带来了种种灾祸,严重的威胁着地球生命生存的生态环境,下列有关减少或者防止酸雨形成的措施中可行的是( )
①对燃煤进行脱硫;②对含SO2、NO2等工业废气进行无害处理后,再排放到大气中;③飞机、汽车等交通工具采用清洁燃料,如天然气、甲醇等。
A. ① B. ② C. ③ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成抗心律失常药物决奈达隆的一种中间体,可通过以下方法合成:
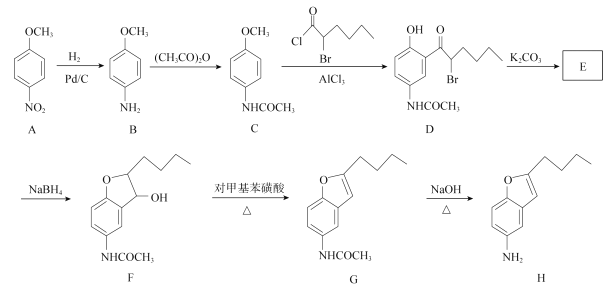
(1))D中的含氧官能团名称为________________(写三种)。
(2)F→G的反应类型为____________。
(3)写出同时满足下列条件的C的一种同分异构体的结构简式:_______________________。
①能发生银镜反应
②能发生水解反应,其水解产物之一能与FeCl3溶液发生显色反应
③分子中只有4种不同化学环境的氢。
(4)E经还原得到F,E的分子式为C14H17O3N,写出E的结构简式:________________________。
(5)已知:
①苯胺(![]() )易被氧化。
)易被氧化。
②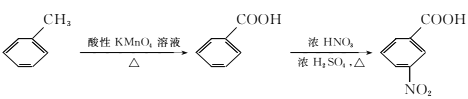
请以甲苯和(CH3CO)2O为原料制备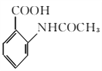 ,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。 ______________________
,写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。 ______________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com