
| A. | 2molA+1molB | B. | 2molA+1molB+3molC+1mol D | ||
| C. | 3molC+1molD | D. | 4molA+2molB+3molC |
分析 恒温恒容下,不同途径达到平衡后,C的浓度仍为W mol/L,说明与原平衡为等效平衡,按化学计量数转化到左边,满足n(A)=4mol,n(B)=2mol即可,据此解答.
解答 解:2A(g)+B(g)  3C(g)+D(g)
3C(g)+D(g)
4mol 2mol 6mol 2mol
A、2molA+1molB与4molA+2molB不相等,在温度、体积不变的情况下不是相同平衡状态,故A错误;
B、开始加入2molA+1molB+3molC+1molD,按化学计量数转化到左边可得4molA、2molB,与原平衡为等效平衡,故B正确;
C、3molC+1molD相当于2molA+1molB,与4molA+2molB不相等,在温度、体积不变的情况下不是相同平衡状态,故C错误;
D、4molA+2molB+3molC与4molA+2molB不相等,在温度、体积不变的情况下不是相同平衡状态,故D错误.
故选B.
点评 本题考查化学平衡的有关计算、等效平衡,难度中等,构建平衡建立的途径是解题关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ②④⑤ | C. | ③⑤⑥ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将wg a%的NaCl溶液蒸发掉w/2g水,得到2a%的NaCl溶液 | |
| B. | 将25g无水CuSO4溶于水制成100mL溶液,其浓度为1mol/L | |
| C. | 将1体积c1mol/L的硫酸用水稀释为5体积,稀溶液的浓度为0.2c1mol/L | |
| D. | 将5.85gNaCl晶体溶入100mL水中,制得0.1mol/L的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
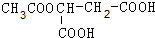 +H2O.
+H2O.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com