
| A. | ①②④⑥⑦ | B. | ④⑥ | C. | ①④⑤⑧ | D. | ①②④⑤⑥⑦ |
分析 一般非金属元素之间形成共价键,由共价键形成的物质在溶于水、化学变化中共价键被破坏,以此来解答.
解答 解:①碘升华,属于物理变化,破坏分子间作用力,故错误;
②溴蒸气被木炭吸附,属于物理变化,破坏分子间作用力,故错误;
③酒精溶于水,属于物理变化,破坏分子间作用力和氢键,故错误;
④HCl气体溶于水,HCl发生了电离,共价键被破坏,故正确;
⑤冰融化,属于物理变化,破坏分子间作用力和氢键,故错误;
⑥NH4Cl受热分解,破坏离子键和共价键,故正确;
⑦氢氧化钠熔化,破坏离子键,故错误;
⑧(NH4)2SO4溶于水,破坏离子键,故错误;
故选B.
点评 本题考查化学键知识,题目难度不大,注意共价键、离子键以及分子间作用力的区别,侧重于考查学生的分析能力.


科目:高中化学 来源: 题型:解答题
| 元素代号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(nm) | 0.186 | 0.160 | 0.152 | 0.153 | 0.110 | 0.099 | 0.075 | 0.074 |
| 主要化合价 | +1 | +2 | +1 | +3 | +5、 -3 | +7、 -1 | +5、 -3 | -2 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点/℃ | 化学性质 |
| H2C2O4 | 189.5℃ | 二元弱酸,有毒,具有腐蚀性,易溶于水,100℃开始升华,157℃时开始分解,与浓硫酸混合加热会产生CO2、CO和H2O,草酸钙和草酸氢钙均为白色不溶物 |
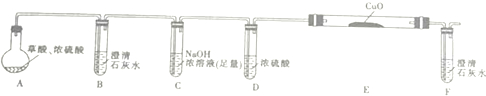
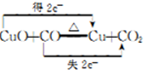
| 编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| Ⅰ | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| Ⅱ | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| Ⅲ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
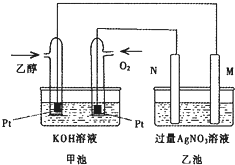 如图是个乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料分别是石墨和铁工作时M、N两个电极的质量都不减少,请回答:
如图是个乙醇燃料电池工作时的示意图,乙池中M、N两个电极的材料分别是石墨和铁工作时M、N两个电极的质量都不减少,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol•L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间的关系可用如图曲线来表示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
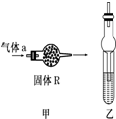 干燥管在不同情况下常具有多种功能.下列两种不同图示就分别代表了干燥管的不同应用.请回答有关问题:
干燥管在不同情况下常具有多种功能.下列两种不同图示就分别代表了干燥管的不同应用.请回答有关问题:| A | B | C | D | |
| 气体a | NH3 | SO2 | C2H4 | Cl2 |
| 固体R | 碱石灰 | 浓硫酸 | 高锰酸钾 | 碱石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中加入盐酸,产生的气体能使石灰水变浑浊,该溶液中一定含有CO32- | |
| B. | 某溶液中加入硝酸酸化的BaCl2,产生白色沉淀,该溶液中一定含有SO42- | |
| C. | 用洁净的铂丝蘸取某溶液在酒精灯上灼烧,产生黄色火焰,溶液中一定含Na+,一定不含K+ | |
| D. | 某溶液中加入NaOH溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,该溶液中一定含有NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com