
【题目】用下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是

A. Ⅰ、Ⅱ装置之间缺少干燥装置 B. CuO没有全部被还原
C. Ⅱ装置中玻璃管内有水冷凝 D. Ⅲ装置后缺少干燥装置
【答案】B
【解析】
试题通氢气前后玻璃管的质量差为反应的CuO中O的质量,反应前后U形管的质量差为反应生成的水的质量。Ⅰ、Ⅱ装置之间没有干燥装置,则使Ⅰ中反应带出的水蒸气进入U形管使水的质量增大,则H质量增加,导致m(H)∶m(O)>1∶8。若Ⅱ装置有水冷凝,则使测得的水的质量减小,设冷凝水质量为m,则H质量减小m/9,但Ⅱ装置质量增加m,即测得O质量减小m,由于m(H)∶m(O)=1∶8,若设m(H)=n,则m(O)=8n,则测得的![]() =
=![]() =
=![]() +
+![]() >
>![]() ,因此测得m(H)∶m(O)>1∶8。Ⅲ装置后缺少干燥装置,会导致CaCl2吸收空气中的水蒸气,导致测得水的质量增加,m(H)∶m(O)>1∶8。只有B中CuO没有被完全还原,则对m(H)∶m(O)的测定没有影响,因此一定错误,所以答案选B。
,因此测得m(H)∶m(O)>1∶8。Ⅲ装置后缺少干燥装置,会导致CaCl2吸收空气中的水蒸气,导致测得水的质量增加,m(H)∶m(O)>1∶8。只有B中CuO没有被完全还原,则对m(H)∶m(O)的测定没有影响,因此一定错误,所以答案选B。


 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源: 题型:
【题目】下列过程中发生了加成反应的是( )
A.C2H4使酸性高锰酸钾溶液褪色
B.C2H4使溴的CCl4溶液褪色
C.C2H4燃烧生成二氧化碳和水
D.CH4和Cl2的混合气体在光照条件下逐渐褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20mL0.5mol L-1的醋酸溶液中逐滴加入等物质的量浓度的烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的相关说法中错误的是
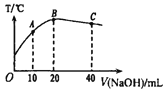
A. 由水电离出的c(H+):C点>B点
B. 醋酸的电离平衡常数:B点> A点
C. 从A点到B点,混合溶液中可能存在:c( CH3COO-) = c(Na+)
D. C 点混合溶液中一定存在:c(Na+) =2c(CH3COO-) +2c(CH3COOH)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaHSO3被用于棉织物和有机物漂白以及在染料、造纸、制革等工业中用作还原剂。
(1)NaHSO3可由NaOH溶液吸收SO2制得。
2NaOH(aq)+SO2(g)==Na2SO3(aq)+H2O(l) ΔH1
2NaHSO3(aq)==Na2SO3(aq)+SO2(g)+H2O(l) ΔH2
则反应SO2(g)+NaOH(aq)==NaHSO3(aq)的ΔH3=__________(用含ΔH1、ΔH2的代数式表示)。
(2)NaHSO3在不同温度下均可被KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3 的反应速率。将浓度均为0.020mol·L-1NaHSO3(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。
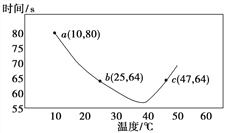
①a点时,v(NaHSO3)=__________mol·L-1·s-1。
②10~40℃区间内,显色时间越来越短,其原因是__________。
(3)已知:t℃时 H2SO3的Ka1=1.5×10-2,Ka2=1.0×10-7;NaHSO3溶液pH<7。在t℃时,往NaOH溶液中通入SO2。
①在NaHSO3溶液中加入少量下列物质后,c(H2SO3)/c(HSO3-)的值增大的是______(填字母);
A.H2O B.稀H2SO4 C.H2O2溶液 D.NaOH溶液
②某时刻,测得溶液的pH=6,则此时,n(HSO3-)/n(SO32-)=_________;
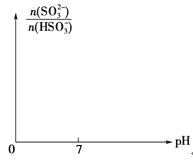
③请画出从开始通入SO2直至过量时,溶液中n(SO32-)∶n(HSO3-)随pH的变化趋势图。_______
(4)以硝酸、硫酸水溶液作电解质进行电解,在汞电极上NO3-可转化为NH2OH,以铂为另一极,则该电解反应的化学方程式_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸氢钠甲醛(NaHSO2HCHO2H2O)俗称吊白块,不稳定,120℃时会分解。在印染、医药以及原子能工业中有广泛应用。以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如下:
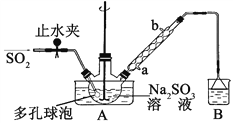
步骤1:在三颈烧瓶中加入一定量Na2SO3和水,搅拌溶解,缓慢通入SO2,至溶液pH 约为4,制得NaHSO3溶液。
步骤2:将装置A 中导气管换成橡皮塞。向烧瓶中加入稍过量的锌粉和一定量甲醛溶液,在80~90℃下,反应约3h,冷却至室温,抽滤;
步骤3:将滤液真空蒸发浓缩,冷却结晶。
(1)装置B 的烧杯中应加入的溶液是____________;冷凝管中冷却水从_____(填“a”或“b”)口进水。
(2)A中多孔球泡的作用是__________________________________________。
(3)冷凝管中回流的主要物质除H2O 外还有________ (填化学式)。
(4)写出步骤2中发生反应的化学方程式________________________________。
(5)步骤3中在真空容器中蒸发浓缩的原因是____________________________。
(6)为了测定产品的纯度,准确称取2.0g样品,完全溶于水配成100mL溶液,取20.00mL所配溶液,加入过量碘完全反应后(已知I2不能氧化甲醛,杂质不反应),加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.466g,则所制得的产品的纯度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左侧充入1 mol N2,右侧充入CO和CO2的混合气体共8 g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是
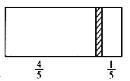
A. 右侧CO与CO2分子数之比为1∶3
B. 右侧气体密度是相同条件下氢气密度的18倍
C. 右侧CO的质量为1.75 g
D. 若隔板处于距离右端1/6处,其他条件不变,则前后两次压强之比为25∶24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物![]() 在医药合成中有着广泛的用途。下列而关该物质的说法正确的是
在医药合成中有着广泛的用途。下列而关该物质的说法正确的是
A. 该化含物中含氧官能团为酯基
B. 该化台物中的所有碳原子一定处于同一平面内
C. 该化合物可发生取代反应、加成反应和氧化反应
D. 该化合物的同分异构体中,苯环上有两个取代基的共3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL 浓度均为0.1mol/L (NH4)2SO4、NH4HSO4混和溶液中滴加0.1mol/L的Ba(OH)2溶液。充分反应后静置,溶液的pH 与所加Ba(OH)2溶液体积的关系如右图,下列说法正确的是
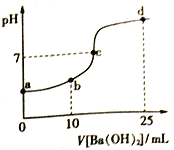
A. a点溶液中: c(NH4+) +c(NH3·H2O)=0.2 mol/L
B. b点溶液中: c(NH4+)>c(SO42-)>c(H+)> c(NH3·H2O)> c(OH-)
C. c点溶液中: c(Ba2+)+ c(NH4+)= c(SO42-)
D. d 点溶液中: c(NH3·H2O)> c(SO42-)>c(NH4+)> c(OH-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知十种物质:①H2O ②空气 ③ Mg ④ CaO ⑤H2SO4 ⑥氢氧化钡 ⑦饱和FeCl3溶液 ⑧氨水 ⑨HNO3 ⑩胆矾,根据上述提供的物质,回答下列问题:
(1)属于混合物的是___________(填序号,下同),属于弱电解质的是_______________。
(2)上述物质中_____与_____在水溶液中可发生反应,且离子方程式为H++OH-===H2O。
(3)实验室制备少量Fe(OH)3胶体所用的物质有____________,反应的离子方程式为_____________________________________________。
(4)实验室配制900mL 0.1mol/L硫酸铜溶液,需要称取的溶质(从上述物质中选取)的质量为________g,从配制好的溶液中取出300mL,其中含有SO42-的数目为_______(设NA为阿伏加德罗常数的值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com