
 若参赛人对此题的信息关系制作一个信息相关图,解题就容易多了,如:
若参赛人对此题的信息关系制作一个信息相关图,解题就容易多了,如:

科目:高中化学 来源:不详 题型:单选题
| A.澄清石灰水 |
| B.水玻璃(Na2SiO3)? |
| C.氢硫酸 |
| D.氯化钙? |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.它溶于水得相应的酸 |
| B.它对应的水化物是可溶性强酸 |
| C.它与强碱溶液反应只生成盐和水 |
| D.它是非金属氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.C60是一种新型的化合物 |
| B.C60和石墨都是碳的同素异形体 |
| C.C60中含离子键 |
| D.C60的式量是720 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Si(粗)+2CO
Si(粗)+2CO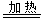 SiCl4
SiCl4 Si(纯)+4HCl
Si(纯)+4HCl| A.①、③是置换反应,②是化合反应 |
| B.高温下,焦炭与氢气的还原性均强于硅 |
| C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子 |
| D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Cu +2H2SO4(浓)  CuSO4 +SO2↑+2H2O CuSO4 +SO2↑+2H2O |
B.Cu +Cl2 CuCl2,CuCl2+ H2SO4(浓) CuCl2,CuCl2+ H2SO4(浓)  CuSO4 +2HCl↑ CuSO4 +2HCl↑ |
C.Cu + H2SO4 +H2O2 CuSO4 +2H2O CuSO4 +2H2O |
D.3Cu +8HNO3=3Cu(NO3)2 +2NO↑+4H2O,Cu(NO3)2+H2SO4(浓)  CuSO4 +2HNO3↑ CuSO4 +2HNO3↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com