
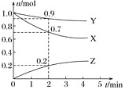
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )
A.X+3Y![]() 2Z 0.1 mol L-1min-1B.2X+Y
2Z 0.1 mol L-1min-1B.2X+Y![]() 2Z 0.1 mol L-1min-1
2Z 0.1 mol L-1min-1
C.X+2Y![]() Z 0.05 mol L-1min-1D.3X+Y
Z 0.05 mol L-1min-1D.3X+Y![]() 2Z 0.05 mol L-1min-1
2Z 0.05 mol L-1min-1
 新课标同步训练系列答案
新课标同步训练系列答案科目:高中化学 来源: 题型:
【题目】烃A的分子量为92且所有碳原子都在同一平面上。一种由烃A制备水杨酸的过程如下∶
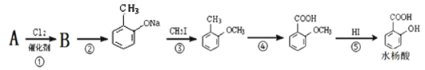
(1)请写出由B生成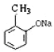 的反应方程式∶_________________________________;
的反应方程式∶_________________________________;
(2)在合成线路中,设计第③和第⑤这两步反应的目的是∶_____________________。
(3)若与水杨酸相关的转化关系如下∶
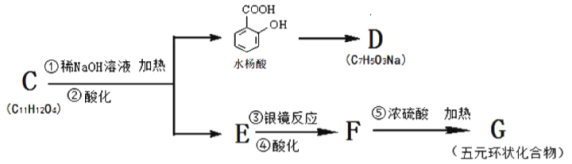
请用一个化学反应证明水杨酸中两官能团酸性差异∶____________________。
(4)①反应类型为∶_________、___________;
(5) G的结构简式为∶___________; 官能团名称∶_____________;
(6)请写出同时符合下列要求的水杨酸的所有同分异构体的结构简式______________。
①滴入FeCl3溶液,发生显色反应;
②能发生银镜反应∶
③苯环上一氯代物有两种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是有机物R 的结构简式,它可用于生产 S﹣诱抗素,下列关于R 的说法正确的是
( )
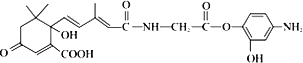
A.R 结构中含手性碳原子数多于 1 个
B.R 可以在酸性条件下充分水解生成两种有机产物
C.R 可以发生氧化、取代、加聚、缩聚反应,并能与盐酸反应生成有机盐
D.1 mol R 分别与足量NaOH 溶液、足量溴水反应,最多消耗 4 mol NaOH 和 5 mol Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应C(s)+H2O(g)![]() CO(g)+H2(g)在密闭容器中进行,一段时间后达到平衡,下列措施不能使平衡发生移动的是( )
CO(g)+H2(g)在密闭容器中进行,一段时间后达到平衡,下列措施不能使平衡发生移动的是( )
①增加C的物质的量 ②保持体积不变,充入N2使体系压强增大 ③将容器的体积缩小一半 ④保持压强不变,充入N2使容器体积变大
A. ①② B. ②③ C. ①④ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 Ksp(AgCl)=1.0×10-12,Ksp(AgI)=1.0×10-16。下列说法正确的是
A.向AgCl饱和溶液中加入少量水,c(Ag+)先减小后增大
B.向0.01mol/L的AgNO3溶液中,加入等体积的浓度均为0.001mol/L的Cl-、I-的混合溶液,只析出AgI沉淀
C.常温下,AgCl沉淀若要在NaI溶液中开始转化为AgI沉淀,则NaI的浓度必须不低于1.0×10-10mol/L
D.向10ml0.1mol/L AgNO3溶液中滴加1ml0.1mol/L的NaCl溶液,有白色沉淀生成,再滴加0.1mol/L的KI溶液,有黄色沉淀生成,说明Ksp(AgCl)> Ksp(AgI)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是( )
A.铝片与稀硫酸的反应
B.Ba(OH)2·8H2O与NH4Cl的反应
C.灼热的炭与CO2的反应
D.甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物W的结构简式为![]() 下列有关W的说法错误的是
下列有关W的说法错误的是
A.是一种酯类有机物B.含苯环和羧基的同分异构体有3种
C.所有碳原子可能在同一平面D.能发生取代、加成和氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的吸收液用三室膜电解技术处理,原理如图所示.下列说法错误的是
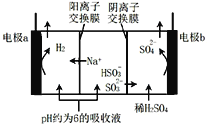
A.电极a为电解池阴极
B.阳极上有反应HSO3—-2e—+H2O=SO42—+3H+发生
C.当电路中通过1mol电子的电量时,理论上将产生0.5mol H2
D.处理后可得到较浓的H2SO4和NaHSO3产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下,830℃时,向一个2 L的密闭容器中充入0.2 mol的A和0.8 mol的B。
C(g)+D(g)反应的平衡常数和温度的关系如下,830℃时,向一个2 L的密闭容器中充入0.2 mol的A和0.8 mol的B。
温度 | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)反应达平衡后,升高温度,平衡_______移动(填“正向”或“逆向”)
(2)830℃达平衡时,A的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com