
(15分)Fe2O3俗称氧化铁红,常用作油漆着色剂。工业以煤矸石(主要成分:SiO2 49.5%;Fe2O3 20.6%;Al2O318.9%,以及MgO、FeO等其他杂质)制备并研究氧化铁红的应用。
(一)制备氧化铁红
1.预处理:将煤矸石粉碎,在350℃下焙烧2小时。
2.加酸溶【解析】
将预处理后的煤矸石溶于质量分数为15%过量的硫酸溶液中,过滤。在滤液中加入的H2O2。
3.调节pH:在上述滤液中加1mol/LNaOH溶液调节溶液的pH,再过滤,得到滤渣。
4.产品处理:将滤渣进行水洗、烘干、煅烧、研磨、过筛得产品。
已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
开始沉淀 | 1.3 | 3.3 | 7.5 | 10.3 |
完全沉淀 | 2.8 | 5.2 | 9.7 | 12.2 |
请回答下列问题:
(1)预处理时,将煤矸石焙烧2小时的目的是 。
(2)酸浸操作中,过量H2SO4的作用是 。
在实验室中进行该操作时,用到玻璃仪器有 、 。
(3)用NaOH溶液调节pH的最佳范围是 。若从第二次过滤的滤液中获取较纯净的硫酸镁晶体,应补充的操作是 、洗涤后,干燥即得。
(4)产品处理时,对滤渣水洗的操作是 。
(二)分析与讨论:


(5)产品处理时,煅烧温度对产品的纯度有很大影响。已知温度对产物纯度的影响如图1所示,则煅烧时温度最好控制在 ℃。
(6)吸油量是反映氧化铁红表面性质的重要指标。吸油量大,说明氧化铁红表面积较大,则用在油漆中会造成油漆假稠,影响质量。不同浓度的两种碱溶液对产物吸油量影响如图2所示,则上述生产中在调节溶液pH时,选用NaOH溶液而不选用氨水的原因是 。
(1)将煤矸石中的矿物转化为氧化物,便于酸浸 (2分)
(2)提高浸取率,抑制Fe3+等水解 (2分)
烧杯、玻璃棒 (各1分)
(3)2.8≤pH<3.3;(2分) 继续加碱调pH至12.2,将沉淀分离并洗净后,溶于足量稀硫酸,再蒸发(浓缩)、冷却(结晶)、过滤 (2分)
(4)加水恰好浸没滤渣,待滤尽后重复2~3次 (2分)
(5)800 (1分)
(6)用NaOH溶液,获得的氧化铁表面积小,吸油量低(2分)
【解析】
试题分析:(1)将煤矸石焙烧2小时,反应充分,可将煤矸石中的矿物转化为氧化物,便于酸浸。
(2)酸浸后生成Fe2(SO4)3,所以过量H2SO4可以提高浸取率,抑制Fe3+等水解。
(3)根据表中数据,Fe3+完全沉淀时的pH为2.8,而Al3+开始沉淀时的pH为3.3,要使Fe3+完全转化为沉淀而不含杂质,调节pH的最佳范围是2.8≤pH<3.3;继续加碱调pH至12.2,Mg2+完全转化为Mg(OH)2沉淀,将沉淀分离并洗净后,溶于足量稀硫酸,再蒸发(浓缩)、冷却(结晶)、过滤,可获取较纯净的硫酸镁晶体。
(4)滤渣水洗的操作是:加水恰好浸没滤渣,待滤尽后重复2~3次。
(5)根据图1曲线,800℃时产品的纯度达到较大值,再升温,纯度升高不大,所以煅烧时温度最好控制在800℃
(6)根据图2两条曲线可知:用NaOH溶液,获得的氧化铁表面积小,吸油量低。
考点:本题考查物质的制备、基本操作、图像的分析。


 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案科目:高中化学 来源:2013-2014江苏省第二学期期中考试高二化学试卷(解析版) 题型:实验题
(20分)某研究性学习小组在实验室中配制0.20mol·L-1的盐酸标准溶液,然后用其滴定某未知浓度的氢氧化钠溶液。
⑴配制待测液:将1.7 g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200 mL溶液,所需的主要玻璃仪器除烧杯,200 mL容量瓶,量筒,还有 ﹑ 。
⑵滴定:
①盛装0.20mol·L-1盐酸标准液应该用 式滴定管,
②滴定时,先向锥型瓶中加酚酞作为指示剂;再逐滴滴定,观察到 时为滴定终点。
③有关数据记录如下:
滴定序号 | 待测液体体积(mL) | 所耗盐酸标准液的体积(mL) | |
起始读数 滴定前 | 终点读数 | ||
1 | 20.00 | 0.50 | 20.40 |
2 | 20.00 | 6.00 | 26.10 |
3 | 20.00 | 4.00 | 24.00 |
数据处理:NaOH溶液的浓度为 mol·L-1,烧碱样品的纯度为 。(保留三位有效数字)
⑶试分析以下各项操作对实验结果的可能影响,用“偏高”﹑“偏低”或“无影响”等填空:
①若用蒸馏水冲洗锥形瓶,则会使测定的结果 ;
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果 ;
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果 ;
④读数时,若滴定前俯视读数,滴定后仰视读数,则会使测定结果 ;
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:选择题
据报道,N4是一种形似白磷的分子,18O2是比黄金还贵重的物质。下列说法正确的是
A. 18O2 与16O2 性质完全相同 B.N4=2N2是化学变化
C. N4和N2互为同位素 D.18O2中含18个中子
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三第三次调研测试化学试卷(解析版) 题型:选择题
锌溴液流电池是一种新型电化学储能装置(如右图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是

A.充电时电极a连接电源的负极
B.放电时负极的电极反应式为Zn—2e-=Zn2+
C.放电时左侧电解质储罐中的离子总浓度增大
D.阳离子交换膜可阻止Br2与Zn直接发生反应
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三第三次调研测试化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.HClO的电子式: B.硫离子结构示意图:
B.硫离子结构示意图:
C.丙醛的结构简式:CH3CH2COH D.碳酸的电离方程式:H2CO3 2H++CO32-
2H++CO32-
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三5月信息卷化学试卷(解析版) 题型:选择题
常温下,下列各溶液的叙述中正确的是
A.NaHSO3与Na2SO3混合溶液中:3c(Na+) = c(HSO3-) + c(SO32-)
B.0.1mol·L-1的醋酸钠溶液20 mL与0.1mol·L-1盐酸10 mL混合后溶液显酸性
c (CH3COO-)>c (Cl-)>c (CH3COOH)>c (H+)
C.等物质的量浓度等体积的NH4HSO4和NaOH溶液混合:
c(Na+)=c(SO42-)>c(NH4+)>c(H+)>c(OH-)
D.向1.00 L 0.3mol·L-1NaOH溶液中缓慢通入0.2molCO2气体,溶液中:
c(Na+) > c(CO32-) > c(HCO3-) > c(OH-) > c(H+)
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省淮安市高三5月信息卷化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.常温下,22gCO2和N2O混合气体中,含有的原子数目为1.5NA
C.标准状况下,2.24L甲醇中含有C—H键的数目为0.3NA
D.a mol·L—1的氯化铁溶液中,若Fe3+的数目为 NA,则Cl—的数目为3NA
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省海门市第一学期期末教学质量调研高一化学试卷(解析版) 题型:选择题
下列各组物质不能实现直接转化的是
A.S→SO2→H2SO4→MgSO4 B.Cu→CuCl2→Cu(NO3)2→Cu(OH)2
C.Al→Al2O3→Al(OH)3→NaAlO2 D.Na→Na2O→Na2CO3→NaCl
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省无锡市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有机反应中,不属于取代反应的是
A.CH4+Cl2  CH3Cl+HCl
CH3Cl+HCl
B.2CH3CHO+O2 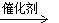 2CH3COOH
2CH3COOH
C.CHCl3+HF CHFCl2+HCl
CHFCl2+HCl
D.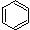 +Br2
+Br2 
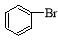 +HBr
+HBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com