
工业碳酸钠(纯度约为98%)中含有Mg2+、Fe2+、Cl-和SO42-等杂质,提纯工艺流程如下:
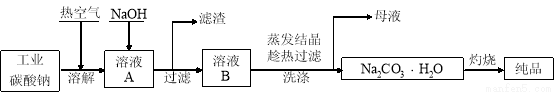
已知:碳酸钠的饱和溶液在不同温度下析出的溶质如下图所示:
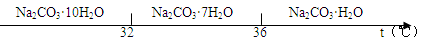
回答下列问题:
(1)溶解时通入热空气的作用有 (写出两条即可);生成氢氧化镁沉淀的离子方程式为 。
(2)“趁热过滤”时的温度应控制在 ;简述过滤后洗涤固体的操作 。
(3)为检验母液中是否含有Cl-,必须加入的试剂为 。
(4)实验室进行“灼烧”的陶瓷仪器有 。
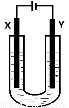
(5)室温下用石墨电极电解饱和Na2CO3溶液(装置如图),写出Y电极反应式: ;一段时间后X电极可收集到的气体一定有 ,可能有 。
(1)升温加快溶解速率、除去铁元素【或加热促进Fe3+(Fe2+)的水解或氧化Fe2+】(2分);Mg2+ +2OH-= Mg (OH) 2↓(或MgCO3 +2OH-= Mg (OH) 2+CO32-) (2分)
(2)不低于36℃(2分);
向过滤器中加入36℃的热水没过固体表面,待水自然流干后,重复操作2~3次(2分)
(3)足量的Ba(NO3)2和HNO3溶液(1分)、少量的AgNO3溶液(1分)
(4)坩埚、泥三角(2分)(答酒精灯不倒扣分,其余答错一个倒扣1分,直到本小问0分)
(5)2H+ +2e- =H2↑(或2H2O +2e- = H2↑+2OH-,2分);O2;CO2(写名称也给分,各1分,共2分)
【解析】
试题分析:(1)溶解时通入热空气可以加快溶解速率,同时可以氧化亚铁离子为铁离子,方便除去铁元素;镁离子与氢氧根离子结合生成氢氧化镁沉淀,离子方程式为Mg2+ +2OH-= Mg (OH) 2↓;
(2)碳酸钠的饱和溶液在不同温度下析出不同的溶质,据图可知,低于36℃时会生成Na2CO3·7H2O等,所以“趁热过滤”时的温度应控制在不能低于36℃;过滤后洗涤固体时不同于一般的洗涤,仍要注意蒸馏水的温度不能低于36℃,所以正确操作是向过滤器中加入36℃的热水没过固体表面,待水自然流干后,重复操作2~3次;
(3)因为溶液中存在SO42-,对Cl-的检验带来干扰,所以在检验Cl-前先除去SO42-,所用试剂是足量的Ba(NO3)2和HNO3溶液,然后在加入硝酸银溶液,观察现象,进行判断;
(4)坩埚有不同的类型,实验室进行“灼烧”的陶瓷仪器有瓷坩埚、泥三角;
(5)Y极是阴极,阳离子放电发生还原反应,电极反应式为2H2O +2e- = H2↑+2OH-,X极为阳极,氢氧根离子放电生成氧气,所以X极产生的气体一定有氧气,X极氢氧根离子放电,导致氢离子浓度增大,所以溶液中的碳酸根离子与氢离子反应会生成二氧化碳气体,因此气体中还可能含有二氧化碳。
考点:考查对工业流程的分析判断,洗涤固体的方法,离子检验,实验室仪器的判断,电解原理的应用


 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:2013-2014学年江西省南昌市高三3月第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列实验的操作、现象和解释或结论都正确的是
| 操作 | 现象 | 解释或结论 |
A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 |
B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 |
C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | Al3++3H2O |
D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+=Cu+2Na+ |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省高三年级模拟考试化学试卷(解析版) 题型:选择题
甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,不满足图示转化关系的是
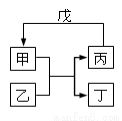
| 甲 | 乙 | 丙 | 戊 |
① | NH3 | O2 | NO | H2O |
② | Fe | H2O | H2 | Fe2O3 |
③ | Al2O3 | NaOH溶液 | Na AlO2溶液 | 过量CO2 |
④ | Na2O2 | CO2 | O2 | Na |
A.①③ B.②③ C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省南京市、盐城市高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.反应SiO2(s)+ 3C(s) = SiC(s) + 2CO(g)室温下不能自发进行,则该反应的△H<0
B.铅蓄电池放电过程中,正极质量增加,负极质量减小
C.25℃下,在NH3·H2O稀溶液中,加水,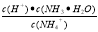 的值不变
的值不变
D.在NaHS溶液中,滴入少量CuCl2溶液产生黑色沉淀,HS-水解程度增大,pH增大
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省南京市、盐城市高三第一次模拟考试化学试卷(解析版) 题型:选择题
下列有关物质性质的应用正确的是
A.氯化钠溶液显中性,可用铝制容器贮存氯化钠溶液
B.碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污
C.氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却
D.铜的金属性比铁弱,可将海轮浸水部分镶上铜锭以减缓船体腐蚀
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省韶关市高三4月高考二模理综化学试卷(解析版) 题型:选择题
下列叙述I和叙述II均正确且有因果关系的是
选项 | 叙述I | 叙述II |
A | H2有还原性,浓硫酸有强氧化性 | 不能用浓硫酸干燥H2 |
B | CuS难溶于水和硫酸 | 反应:H2S+CuSO4=CuS↓+H2SO4可以发生 |
C | 海水中含有大量的Cl-、Br-等离子 | 向海水中通入F2可大量获得Cl2、Br2 |
D | SO2具有酸性和漂白性 | 往紫色石蕊溶液中通入SO2,溶液先变红再褪色 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省茂名市高三第二次高考模拟理综化学试卷(解析版) 题型:填空题
工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收铜和铬等金属,回收流程如下:
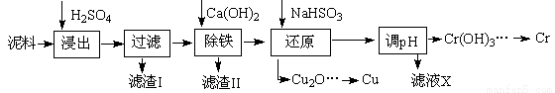
已知部分物质沉淀的pH及CaSO4的溶解度曲线如下:
| Fe3+ | Cu2+ | Cr3+ |
开始沉淀pH | 2.1 | 4.7 | 4.3 |
完全沉淀pH | 3.2 | 6.7 | a |
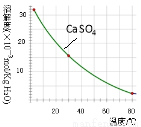
(1)在浸出过程中除了生成Fe2(SO4)3、Cr2(SO4)3外,主要还有
(2)在除铁操作中,需要除去Fe3+和CaSO4,请完成相关操作:①加入石灰乳调节pH到 ;②将浊液加热到80℃, 。
(3)写出还原步骤中加入NaHSO3生成Cu2O固体的离子反应方程式 ,此步骤中加入NaHSO3得到Cu2O的产率为95%,若NaHSO3过量,除了浪费试剂外,还会出现的问题是 。
(4)当离子浓度≤1×10—5 mol?L-1认为沉淀完全,若要使Cr3+完全沉淀则要保持C(OH—)≥ 。已知:Ksp[Cr(OH)3]=6.3×10-31,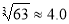 )
)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省肇庆市高三级第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式,不正确的是
A.工业上可用电解法制备Mg:MgCl2(熔融) 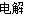 Mg + Cl2↑
Mg + Cl2↑
B.向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+H2O+CO2=2HClO+CaCO3↓
C.用CaSO4治理盐碱地:CaSO4(s) + Na2CO3(aq) CaCO3(s) + Na2SO4(aq)
CaCO3(s) + Na2SO4(aq)
D.用FeSO4除去酸性废水中的Cr2O72-:Cr2O72- + Fe2+ + 14H+ == 2Cr3+ + Fe3+ + 7H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省深圳市高三第二次调研考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.甲苯是饱和烃,氯乙烯是不饱和烃
B.石油的裂化产品能使溴水褪色
C.蛋白质在CuSO4溶液中发生盐析
D.油脂在NaOH溶液中水解生成高级脂肪酸和甘油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com