
���� X��Y��Z��W��L��M���ֶ���������Ԫ�ص�ԭ��������������W�ǵؿ��к������Ľ���Ԫ�أ���WΪAlԪ�أ�L�ĵ��ʾ����۵�ߡ�Ӳ�ȴ���һ����Ҫ�İ뵼����ϣ�LΪSiԪ�أ�Y��ԭ������������������Ӳ�����2����ԭ������С��AlԪ�أ���Y���ڵڶ����ڣ�����������Ϊ4����YΪ̼Ԫ�أ�X��M�ĵ����ڳ����³���̬��X��ԭ������С��CԪ�أ���XΪ��Ԫ�أ�M��ԭ���������ڹ�Ԫ�أ���MΪClԪ�أ�Z��ͬ���ڵ�����Ԫ����ԭ�Ӱ뾶�����IA�壬ԭ����������̼����ZΪNaԪ�أ��ݴ˽��
��� �⣺X��Y��Z��W��L��M���ֶ���������Ԫ�ص�ԭ��������������W�ǵؿ��к������Ľ���Ԫ�أ���WΪAlԪ�أ�L�ĵ��ʾ����۵�ߡ�Ӳ�ȴ���һ����Ҫ�İ뵼����ϣ�LΪSiԪ�أ�Y��ԭ������������������Ӳ�����2����ԭ������С��AlԪ�أ���Y���ڵڶ����ڣ�����������Ϊ4����YΪ̼Ԫ�أ�X��M�ĵ����ڳ����³���̬��X��ԭ������С��CԪ�أ���XΪ��Ԫ�أ�M��ԭ���������ڹ�Ԫ�أ���MΪClԪ�أ�Z��ͬ���ڵ�����Ԫ����ԭ�Ӱ뾶�����IA�壬ԭ����������̼����ZΪNaԪ�أ�
��1��������������֪��LΪSiԪ�أ���Z���ƣ�Ԫ�ص�������ɫ��ӦΪ��ɫ��
�ʴ�Ϊ��Si����ɫ��
��2���ǽ�����Si��C��Cl������ۺ����������������ǿ��˳��ΪH2SiO3��H2CO3��HClO4��
�ʴ�Ϊ��H2SiO3��H2CO3��HClO4��
��3��Z��W���Ե�����������Ӧ��ˮ����ֱ�ΪNaOH��Al��OH��3�����߷�Ӧ����ƫ��������ˮ����Ӧ�����ӷ���ʽΪ��Al��OH��3+OH-�TAlO2-+2H2O��
�ʴ�Ϊ��Al��OH��3+OH-�TAlO2-+2H2O��
��4��R��̼Ԫ��ͬ���ڣ�R�ĵ��ʷ���R2����3�����ۼ�����RΪ��Ԫ�أ�NԪ����SiԪ��һ���������ǽ������ϣ��仯ѧʽ��Si3N4��
�ʴ�Ϊ��Si3N4��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���Ĺؼ����Ƕ�ѧ���ۺ������Ŀ��飬ע�����֪ʶ���������գ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3��3-����-1-��ϩ | B�� | 2��2-����-2-��ϩ | ||
| C�� | 2��2-����-3-��Ȳ | D�� | 3��3-����-1-��Ȳ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
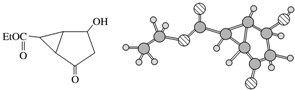
| A�� | ���л��ﲻͬ��ѧ��������ԭ����8�� | |
| B�� | ���л������ڷ����廯���� | |
| C�� | ����ʽ�е�Et�����Ļ���Ϊ-CH3 | |
| D�� | ���л���ķ���ʽΪC9H10O4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����£�78 g ����Na2O2�У����е�������������Ϊ4 NA | |
| B�� | ��״���£�4.48L HF�����к�0.2NA��H-F�� | |
| C�� | ���³�ѹ�£�8gO2����8NA������ | |
| D�� | 4��ʱ��20 g 2H216O�к��й��õ��Ӷ���Ϊ2 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.4 mol/L | B�� | 0.6 mol/L | C�� | 0.8 mol/L | D�� | 1.0 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
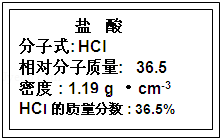
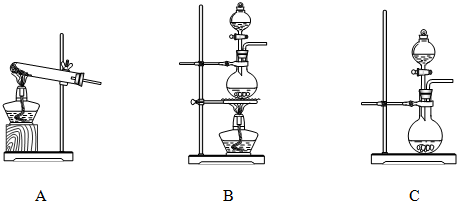

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ǻ�ѧ�仯 | |
| B�� | ����������ͭϡ��Һ��Ӧ���û�����ɫ��ͭ | |
| C�� | ����ʱ������ʹҺ���������ƿ�Ŀ̶��ߣ����������� | |
| D�� | ��������������ֱ���糡�У�һ��ʱ�������������ɫ���˵����������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com