
下列关于硅的说法,不正确的是( )
A.光导纤维的主要成分是二氧化硅
B.二氧化硅是硅酸的酸酐,但不可以用它和水直接反应来制取硅酸
C.硅的化学性质不活泼,但在常温下也可和某些物质反应
D.盛放硅酸钠溶液的试剂瓶不能用玻璃塞的主要原因是硅酸钠溶液水解呈碱性
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016-2017学年安徽省高一上期中化学卷(解析版) 题型:实验题
(1)实验室配制500mL 0.2 mol·L-1 FeSO4溶液,需要称量FeSO4·7H2O__________g。
若实验遇到下列情况,对FeSO4溶液的物质的量浓度有何影响?(填“偏高”“偏低”或“不变”)
①用以溶解FeSO4·7H2O烧杯未洗涤,_______________。
②摇匀后发现液面低于刻度线再加水,_________________。
(2)把少量Na2O2投入含有HCO3-、CO32-、S2-、Na+的溶液中,上述溶液中离子数目增加的是________,离子数目减少的是____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是
A.强酸跟强碱的反应热一定是中和热
B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g) 2NH3(g) ΔH=-38.6kJ/mol
2NH3(g) ΔH=-38.6kJ/mol
C.吸热反应的发生都需要加热,放热反应在常温下一定容易发生
D.表示中和热的离子方程式为H+(aq)+OH-(aq) H2O(l) ΔH=-57.3kJ/mol
H2O(l) ΔH=-57.3kJ/mol
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.体心立方是金属最密堆积的形式
B.在SiO2晶体中,并不存在单个“SiO2”分子
C.干冰中,与CO2分子等距紧邻的CO2分子有8个
D.31 g P4含有P-P键的个数为4NA
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
绿色电源“二甲醚【(CH3)2O】—氧气燃料电池”的工作原理如下图所示,下列说法正确的是( )
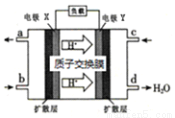
A.氧气应从c处通入,电极Y上发生的反应为:O2+4e-+2H2O=4OH-
B.电池在放电过程中,电极X周围溶液的pH增大
C.当该电池向外电路提供2 mol电子时消耗O2约为11.2L
D.二甲醚应从b处加入,电极X上发生的反应为:(CH3)2O-12e-+3H2O=2CO2+12H+
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上月考三化学试卷(解析版) 题型:推断题
[化学——选修3:物质结构与性质]
A、B、C、D、E、F代表6种元素.请填空:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为 ;
(2)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,E的元素号为 ,其正二价的电子排布式为 .
(3)F元素的原子最外层电子排布式为nsnnpn+1,则n= ;原子中能量最高的是 电子.
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上月考三化学试卷(解析版) 题型:选择题
标准状况下,将体积为V L的圆底烧瓶中充满氨气,倒扣在含有足量水的水槽中(如图所示),实验完毕后立即将烧瓶从水槽中取出,所得溶液的密度为ρg·cm﹣3。下列说法错误的是
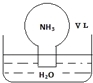
A.水最终会充满整个烧瓶
B.所得溶液的物质的量浓度为 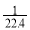 mol·L﹣1
mol·L﹣1
C.所得溶液的质量分数为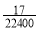 ρ
ρ
D.所得溶液中,n(NH3·H2O)+n(NH4+)=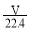 mol
mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高一上期中化学卷(解析版) 题型:实验题
实验室需要配制0.5mol?L-1的烧碱溶液480 mL,根据溶液配制的过程,回答下列问题:
(1)配制该溶液时,使用的玻璃仪器是烧杯、玻璃棒、量筒、 、 ,容量瓶在使用前必须进行的一步操作是 。
(2)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧冷却,其正确的操作顺序为 ,称量时应称取烧碱的质量为 。
(3)在配制过程中,下列操作对所配溶液浓度的影响是(填偏高、偏低或无影响)
①配制前,容量瓶内有水_________
②溶液未冷却便定容__________
③定容时仰视刻度线__________
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一上11月月考化学卷(解析版) 题型:选择题
阿伏伽德罗常数约为6.02×1023mol-1,下列叙述中正确的是
①1.01×105Pa、25℃时,2.24LCl2中含有的原子数为0.2NA
②0.1L3mol﹒L-1NH4NO3溶液中含有的N原子数目为0.3NA
③5.6g铁粉和足量的硫酸铜溶液反应生成的铜原子数为NA
④常温常压下,46gNO2和N2O4的混合物中含有的原子数为3NA
⑤1molNH3所含有的电子数为17NA
⑥1mol/LNaCl溶液中所含的Na+数为NA
⑦常温常压下,28g氮气所含的原子数为2NA
⑧标准状况下,22.4L水所含有的分子数目为NA
A.①④⑤ B.②③⑥⑦ C.④⑦ D.⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com