
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
A.①③ B.①④
C.②④ D.②③
科目:高中化学 来源: 题型:
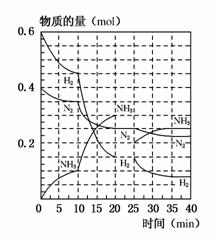
500 ℃、20 MPa时,将H2和N2置于一容积为2 L的密闭容器中发生反应。反应过程中H2、N2和NH3物质的量变化如图所示(10 min时达到第一次平衡),下列说法正确的是( )
A.反应开始到第一次平衡时,N2的平均反应速率为0.005 mol/(L·min)
B.从曲 线可以看出,反应进行到10 min至20 min时可能是使用了催化剂
线可以看出,反应进行到10 min至20 min时可能是使用了催化剂
C.从曲线可以看出,反应进行至25 min时,增加了0.1 mol 的氨气
D.在25 min时平衡正向移动但达到新平衡后NH3的体积分数比原平衡小
查看答案和解析>>
科目:高中化学 来源: 题型:
煤炭燃烧过程中会释放出大量的SO2,严重破坏生态环境。采用一定的脱硫技术可以把硫元素以CaSO4的形式固定,从而降低SO2的排放。但是煤炭燃烧过程中产生的CO又会与CaSO4发生化学反应,降低了脱硫效率。相关反应的热化学方程式如下:
CaSO4(s)+CO(g)CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ·mol-1(反应Ⅰ)
CaSO4(s)+4CO(g)CaS(s)+4CO2(g)
ΔH2=-175.6 kJ·mol-1(反应Ⅱ)
请回答下列问题:
(1)反应Ⅰ能够自发进行的反应条件是________。
(2)对于气体参与的反应,表示平衡常数Kp时用气体组分(B)的平衡压强p(B)代替该气体物质的量的浓度c(B),则反应Ⅱ的Kp=________(用表达式表示)。
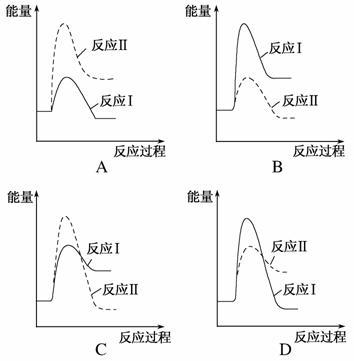
(3 )假设某温度下,反应Ⅰ的速率(v1)大于
)假设某温度下,反应Ⅰ的速率(v1)大于 反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是________。
反应Ⅱ的速率(v2),则下列反应过程能量变化示意图正确的是________。
(4)通过监测反应体系中气体浓度的变化可判断反应Ⅰ和Ⅱ是否同时发生,理由是____________________________________________________ ______________________________________________________________________________________
(5)图1为实验测得不同温度下反应体系中CO初始体积百分数与平衡时固体产物中CaS质量百分数的关系曲线。则降低该反应体系中SO2生成量的措施有________。
A.向该反应体系中投入石灰石
B.在合适的温度区间内控制较低的反应温度
C.提高CO的初始体积百分数
D.提高反应体系的温度
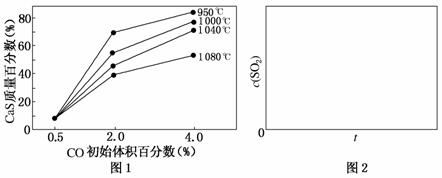
(6)恒温恒容条件下,假设反应Ⅰ和Ⅱ同时发生,且v1>v2,请在图2中画出反应体系中c(SO2)随时间t变化的总趋势图。
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合溶液中含有等物质的量的CuSO4、FeSO4、Fe2(SO4)3。已知下表数据:
| 物质(25℃) | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 完全沉淀时的pH | ≥6.4 | ≥9.6 | 3~4 |
下列叙述正确的是( )
A.混合溶液中:c(SO )[c(Cu2+)+c(Fe2+)+c(Fe3+)]=54
)[c(Cu2+)+c(Fe2+)+c(Fe3+)]=54
B.若向混合溶液中加入铁粉,不可能观察到红色固体析出
C.若向混合溶液中加入足量氯水,调节pH到3~4后过滤,得到纯净的CuSO4溶液
D.若向混合溶液中逐滴加入烧碱溶液,首先生成Fe(OH)3沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化曲线如图所示。下列分析错误的是( )
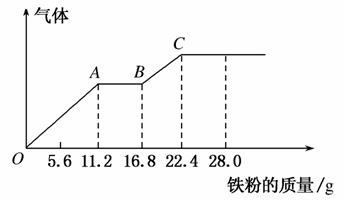
A.AB段的反应为:Fe+2Fe3+===3Fe2+
B.第二份溶液中最终溶质为FeSO4
C.混合酸中NO 物质的量为0.4 mol
物质的量为0.4 mol
D.混合酸中H2SO4浓度为5 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列有关NA的叙述中正确的是 ( )
A.惰性电极电解饱和食盐水,若电路中通过NA个电子,则阳极产生气体11.2L
B.标准状况下,4.0 g CH4中含有共价键的数目为NA
C.1 mol C12发生化学反应,转移的电子数必为2NA
D.在反应KIO3+6HI =KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列按纯净物、混合物、电解质和非电解质顺序排列的是 ( )
A.盐酸、空气、醋酸、干冰 B.冰醋酸、福尔马林、硫酸钠、乙醇
C.蛋白质、油脂、苛性钾、石灰石 D.胆矾、漂白粉、氯化钾、硫酸钡
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如下表所示:
| 检测次数 | 溶液中检测出的物质 |
| 第1次 | KCl、K2SO4、Na2CO3、NaCl |
| 第2次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第3次 | Na2SO4、KCl、K2CO3、NaCl |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com