
| A. | ①②③④ | B. | ①③④⑤ | C. | ②④⑤⑥ | D. | ②③④⑥ |
分析 ①碳酸氢盐加热易分解,碳酸钙高温分解,而碳酸钠性质稳定;
②元素的非金属性越强,对应离子还原性越弱;同一个氧化还原反应中还原剂的还原性>还原产物的还原性;
③铁离子氧化性最强,其它离子可结合金属活动顺序表判断;
④酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子;
⑤元素的非金属性越强,对应的最高价氧化物的酸性越强;
⑥碳酸钙、氢氧化钙微溶于水,碳酸钙难溶,硝酸钙易溶于水.
解答 解:①碳酸氢盐加热易分解,碳酸钙高温分解,而碳酸钠性质稳定,热稳定性应为Ca(HCO3)2<NaHCO3<CaCO3<Na2CO3,故错误;
②元素的非金属性Br>I>S,对应离子还原性S2->I->Br-,又碘离子能将三价铁还原成二价铁,而溴离子不能,所以还原性I->Fe2+>Br-,则还原性S2->SO32->I->Fe2+>Br->Cl-,故正确;
③铁离子氧化性最强,其它离子可结合金属活动顺序表判断,氧化性为Fe3+>Cu2+>H+>Fe2+>Zn2+>Mg2+,故正确;
④酸性越弱,酸越难电离,对应的酸根离子越易结合氢离子,则结合H+的能力:OH->AlO2->CO32->HCO3->CH3COO -,故正确;
⑤非金属性Cl>S>C>Si,元素的非金属性越强,对应的最高价氧化物的酸性越强,故错误;
⑥碳酸钙、氢氧化钙微溶于水,碳酸钙难溶,硝酸钙易溶于水,则溶解度:CaSO4>CaCO3,Ca(NO3)2>Ca(OH)2,故正确.
故选D.
点评 本题考查元素周期律知识,为高考常见题型,侧重于基础知识的考查,注意把握元素周期律的递变规律等,把握比较角度,难度不大.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 相同条件下,H2O电解产物H2和O2的物质的量之比为2:1 | |
| B. | 相同条件下,H2O电解产物H2和O2的质量之比为2:1 | |
| C. | 相同条件下,1molH2与1molO2的体积相同 | |
| D. | 相同条件下,1molH2与1molO2的质量不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| B. | 常温下氯气与烧碱溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 铜与稀硝酸反应:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| D. | 过量的SO2通入NaOH中:SO2+2OH-═SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴苯中含有溴单质,可用NaOH溶液洗涤,再经分液而除去 | |
| B. | 制硝基苯时,在浓硫酸中加入浓硝酸后,立即加苯混合,进行振荡 | |
| C. | 在酸性高锰酸钾溶液中滴加几滴苯,用力振荡,紫红色褪去 | |
| D. | 在液体苯中通氢气可制得环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
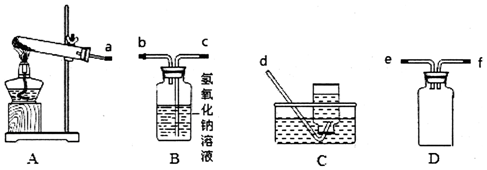
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | LiH、LiD、LiT互为同素异形体 | |
| B. | LiH、LiD、LiT中氢元素的化合价均为+1 | |
| C. | H、D、T互为同位素 | |
| D. | H、D、T的物理性质与化学性质都相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过化学变化可以实现16O与18O之间的转化 | |
| B. | 因为H2O的沸点高于H2S,所以O原子得电子能力大于S原子 | |
| C. | 某化合物熔融状态下能导电,该化合物中一定有离子键 | |
| D. | 化学键是相邻分子之间的强烈的相互作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
| E | 基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
 ,其原子核外有3个未成对电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃形.
,其原子核外有3个未成对电子,能量最高的电子为2p轨道上的电子,其轨道呈哑铃形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的化学方程式为:CO2+H2$?_{高温}^{催化剂}$ CO+H2O | |
| B. | 恒温下缩小容积,平衡不发生移动,H2的浓度也不变 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应的反应热为负值 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com