
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 8.4 L | B. | 11.2 L | C. | 14.0 L | D. | 16.8 L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 分别加入碘化钾溶液,观察颜色变化 | |
| B. | 分别加热,观察是否生成沉淀 | |
| C. | 分别滴加浓硝酸 | |
| D. | 分别灼烧,闻味道 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 已知FeO4n-中Fe的化合价是+6价,则n=2 | |
| B. | 每产生1molCl-,转移2mol电子 | |
| C. | FeO4n-具有强氧化性,一般其还原产物为Fe3+,可用作新型自来水消毒剂和净水剂 | |
| D. | 若n=2,该反应中氧化剂与还原剂的物质的量之比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室制取乙酸乙酯的主要步骤如下
实验室制取乙酸乙酯的主要步骤如下| 物质 | 乙醇 | 乙酸 | 乙酸乙酯 | 浓硫酸 |
| 熔(℃) | -117.0 | 16.6 | -83.6 | ------ |
| 沸(℃) | 78.0 | 117.9 | 77.5 | 338.0 |
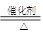 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
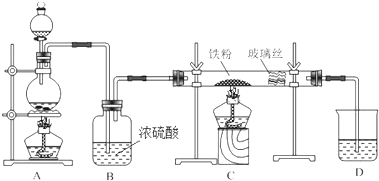
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
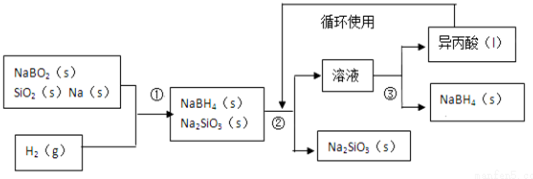
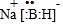 ;其中B元素的化合价为+3
;其中B元素的化合价为+3查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com